Terapia cu celule stem este unul dintre cele mai promițătoare domenii ale medicinei moderne, însă în Statele Unite rămâne strict reglementată. Mulți pacienți se întreabă: Este legală terapia cu celule stem în SUA? Răspunsul scurt este da — dar doar în cazuri specifice și limitate. În acest articol, vom explica regulile, de ce restricțiile sunt încă în vigoare și unde pacienții pot căuta în siguranță tratament în străinătate.

Ce este terapia cu celule stem?
Terapia cu celule stem utilizează cele mai puternice mecanisme de reparare ale organismului — celule specializate și semnalele bioactive pe care acestea le eliberează — pentru a reduce inflamația, a stimula regenerarea și a restabili funcțiile acolo unde medicina convențională se dovedește adesea ineficientă.
Mai degrabă decât să înlocuiască tratamente consacrate, precum chirurgia, medicația sau reabilitarea, această terapie le completează, accelerând recuperarea, îmbunătățind mobilitatea și sporind calitatea vieții. Pentru mulți pacienți, ea oferă o cale alternativă spre recuperare atunci când metodele convenționale singure nu sunt suficiente.
Tipuri de celule stem utilizate în tratamente
Diferite clinici pot folosi surse celulare diferite; la Swiss Medica folosim exclusiv celule stromale mezenchimale adulte multipotente (MSC) și derivatele acestora.
- Celule alogenice: celule provenite de la donatori, din cordonul ombilical sau placentă (colectate după naștere). Sunt intens studiate pentru efectele lor imunomodulatoare și antiinflamatoare.
- Celule autologe: celulele proprii ale pacientului, prelevate din măduva osoasă — sau, în cazuri specifice, din țesutul adipos.
- Derivate fără celule (ex. exosomi/secretom): mesageri biologici care pot fi utilizați împreună cu celulele sau ca protocoale independente în cazurile mai ușoare.
Nu folosim celule embrionare sau celule iPSC.
Este tratamentul cu celule stem legal în SUA în 2025?
Da, terapia cu celule stem este legală în SUA, dar numai atunci când utilizează produse aprobate de FDA pentru afecțiuni medicale specifice. Aprobarea FDA este cea care conferă unui tratament statut legal la nivel federal. Fără această aprobare, procedurile rămân experimentale și nu pot fi oferite ca terapii consacrate, chiar dacă unele state permit utilizarea lor limitată.
Deși multe titluri și materiale publicitare creează impresia unui acces larg, în realitate accesul depinde de două niveluri de reglementare:
- Reguli federale sub egida Administrației pentru Alimente și Medicamente din SUA (FDA).
- Legi la nivel de stat, care pot introduce excepții, dar nu pot înlocui autoritatea federală.
Ca urmare, gama de tratamente cu celule stem legale în SUA este, de fapt, mult mai restrânsă decât sugerează numeroase reclame, concentrându-se în principal pe opțiunile aprobate de FDA.
De exemplu, noul statut din Florida permite medicilor licențiați (MD și DO) să ofere anumite proceduri celulare neaprobate în domeniul tratamentului rănilor, managementului durerii și ortopediei — cu condiția respectării stricte a regulilor de documentare și consimțământ. Texas și Utah au stabilit căi similare. Aceste schimbări arată că peisajul terapiei cu celule stem se îndreaptă treptat către o accesibilitate mai mare pentru pacienți.
Căi pentru a face transplanturile cu celule stem legale în Statele Unite
Înainte ca orice nou tratament cu celule stem să poată fi oferit pe scară largă în SUA, acesta trebuie să parcurgă pași legali și de reglementare specifici. Pentru a fi legal la nivel federal, fiecare nouă terapie cu celule stem trebuie să treacă prin următoarele etape:
| Etapă | Proces | Ce înseamnă pentru pacienți |
| 1 → Categoria specială (361 HCT/Ps) | Unele produse simple pe bază de celule stem pot fi utilizate imediat dacă respectă reguli stricte. | Disponibile doar în cazuri foarte limitate. |
| 2 → Studii clinice | Noile terapii sunt testate mai întâi în studii aprobate de FDA. | Pacienții pot participa la studii pentru a încerca tratamentele din timp. |
| 3 → Utilizare compasională | În cazuri rare, grave sau care pun viața în pericol, pacienții pot solicita o permisiune specială. | Oferă acces atunci când nu există alte opțiuni. |
| 4 → Aprobarea completă de către FDA | FDA analizează toate datele și aprobă oficial terapia. | Tratamentul devine larg disponibil ca opțiune standard în SUA. |
Ce permite de fapt FDA pentru terapia cu celule stem în 2025
FDA reglementează terapiile cu celule stem în principal prin două cadre:
| Produs | Exemplu |
| Produse celulare aprobate (351 HCT/Ps) Necesită studii clinice, cerere de licență biologică (BLA) și producție conform GMP, cu controale stricte de calitate. | Transplantul de celule stem din sânge de cordon ombilical, utilizat în spitalele din SUA pentru a restabili funcția sanguină și imunitară la pacienți cu leucemii, limfoame și alte boli hematologice grave (trebuie să respecte GMP și testări extinse). Terapia CAR-T aprobată de FDA pentru anumite tipuri de leucemii și limfoame. |
| 361 HCT/Ps (mai puțin reglementate) Nu necesită aprobare de piață dacă produsul este minim manipulat, utilizat în scopuri omoloage și respectă toate standardele de siguranță/testare. | Filtrarea celulelor stem din țesutul adipos fără modificarea caracteristicilor lor biologice. Utilizarea celulelor din măduva osoasă pentru a produce celule sanguine (nu pentru a repara cartilajul). |
| 351 HCT/Ps (dacă nu sunt îndeplinite criteriile 361) Reglementate ca medicamente/biologice, necesitând întregul parcurs: studii clinice și aprobare BLA. | Orice produs celular care este substanțial manipulat sau utilizat în scopuri neomoloage trebuie să urmeze întregul proces de aprobare FDA. |
De ce este terapia cu celule stem încă restricționată în Statele Unite — și ce înseamnă pentru pacienți
Chiar dacă terapia cu celule stem promite rezultate la nivel mondial, utilizarea ei în SUA este încă strict restricționată. Pacienții întreabă adesea online: „De ce este ilegală terapia cu celule stem în Statele Unite?” Răspunsul se află într-un amestec de dezbateri etice, cerințe stricte ale FDA privind studiile clinice și întrebări persistente despre siguranța pe termen lung.
Îngrijorări etice
Dezbaterile legate de celulele derivate din embrioni au dus în trecut la bariere stricte. Deși majoritatea clinicilor moderne folosesc MSC-uri, care, în general, nu ridică aceleași probleme etice sau de siguranță ca celulele stem embrionare, legiuitorii încă elaborează reguli ample pentru a evita zonele gri.
Ca urmare, unele terapii rămân oficial încadrate ca ilegale în Statele Unite. Acest lucru se face parțial pentru a preveni utilizarea abuzivă a celulelor embrionare și pentru a opri clinicile să ofere celule care nu sunt procesate conform standardelor stricte ale FDA.
Lipsa studiilor clinice
Principala limitare astăzi este nivelul de dovezi clinice formale pe care autoritățile de reglementare le cer. Pentru noile produse celulare, FDA solicită studii ample, bine controlate. Multe dintre tratamentele pe care oamenii le caută atunci când întreabă „terapii cu celule stem legale în SUA” nu sunt încă pe deplin aprobate, deoarece se află încă în faza de cercetare.
Pentru a acorda aprobare completă, FDA și alte autorități cer studii pe scară largă, pe termen lung, care durează ani de zile. Până atunci, terapia cu celule stem rămâne într-o categorie „restricționată”, chiar dacă clinicile moderne aplică deja standarde și tehnologii recunoscute la nivel internațional.
Provocări legate de eficacitate
Deși dovezile actuale sunt încă insuficiente pentru a formula concluzii științifice definitive cu privire la eficacitatea generală a terapiei cu celule stem, pacienți din întreaga lume continuă să raporteze îmbunătățiri semnificative — mobilitate mai bună, reducerea durerii și restaurarea funcțiilor.
Swiss Medica a documentat sute de astfel de cazuri, cu date de urmărire care susțin aceste rezultate. Unele dintre ele sunt cu adevărat schimbătoare de viață:
- Mers neasistat în câteva săptămâni de la tratament, chiar și după ani de dependență de cadre sau bastoane.
- Reducerea marcată a durerii cronice, cu mențiunea posibilității de a dormi întreaga noapte fără disconfort.
- Îmbunătățiri ale controlului vezicii urinare și ale altor funcții, în unele cazuri ajungând la 30–35% în câteva luni.
Ce înseamnă acest lucru pentru pacienți
Înțelegerea căilor legale este esențială pentru oricine ia în considerare terapia cu celule stem în SUA.
FDA reglementează tratamentele foarte strict, iar multe terapii cu profil de siguranță deja demonstrat în alte țări nu sunt încă disponibile în Statele Unite, pur și simplu pentru că nu au parcurs încă procesul lung de aprobare.
Lipsa aprobării FDA nu înseamnă că aceste proceduri sunt dăunătoare. Cel mai adesea, aceasta înseamnă pur și simplu că cercetarea este încă în desfășurare, ca în cazul oricărui produs inovator.
Ce se întâmplă dacă primiți tratament într-o clinică nereglementată?
Transplanturile legitime de celule stem, cu căi legale în Statele Unite (precum transplanturile de sânge din cordonul ombilical pentru afecțiuni hematologice), există deoarece respectă standarde stricte. Problema apare pe piața nereglementată: până în 2021, cercetătorii au documentat peste 2.700 de clinici în SUA care vindeau tratamente cu celule stem neaprobate. Aceste clinici operează în afara supravegherii FDA, se bazează pe surse celulare nevalidate și ignoră standardele de siguranță de bază — ceea ce a dus deja la multiple avertismente din partea FDA și chiar la procese în instanță.
Acoperirea mediatică negativă creează adesea impresia că toate clinicile sunt la fel. În același timp, FDA nu face suficient pentru a informa publicul despre cercetările în desfășurare, ceea ce lasă un gol de informare. Ca urmare, oamenii fie resping tratamente care ar putea fi utile, fie se confruntă cu dificultăți în a înțelege cum să aleagă o clinică de încredere.
Care poate fi soluția? Deși terapia cu celule stem ar putea primi aprobarea FDA în viitor, mai multe tratamente promițătoare sunt deja disponibile în clinici autorizate din străinătate. Pentru pacienții care nu doresc să aștepte ani întregi procesul de aprobare din SUA, o clinică internațională transparentă și bine reglementată poate fi o alternativă sigură și eficientă.
Clinicile de renume din străinătate funcționează sub reglementări naționale stricte, respectă standardele de producție GMP și utilizează terapii care au fost evaluate și aprobate de autoritățile locale de sănătate — chiar dacă acestea așteaptă încă revizuirea FDA.
Turism medical pentru terapia cu celule stem: Merită?
Confruntați cu complexitatea din propria țară, mulți americani se întreabă adesea: „De ce sunt celulele stem ilegale în Statele Unite, comparativ cu alte locuri?” Această confuzie îi determină adesea să analizeze turismul medical reglementat, unde căile legale și aprobările sunt mai clare.
Este legal să călătorești pentru tratament cu celule stem?
Fiecare cetățean american are dreptul de a călători liber în străinătate și de a lua decizii independente privind tratamentul medical, inclusiv primirea de îngrijiri medicale. Acest drept se bazează pe dreptul constituțional la libertatea de mișcare și pe principiul consimțământului informat, consacrat în jurisprudența americană.
Totuși, în unele țări unde terapia cu celule stem este legală, regulile echivalente celor din SUA nu se aplică, iar pacienții pot accesa tratamente mai rapid, dar cu mai puțină supraveghere — ceea ce face ca verificarea clinicii să fie esențială.
Ce ar trebui să verifice un pacient înainte de a ajunge la clinică?
- Reglementarea în țara de destinație — verificați dacă terapia pe care o căutați este legală și reglementată oficial.
- Credibilitatea clinicii — asigurați-vă că clinica este licențiată, are un istoric medical și respectă standardele locale de sănătate.
De ce mulți americani aleg tratamentul cu celule stem în străinătate
Pentru pacienții care nu doresc să aștepte ani întregi aprobarea FDA, apar destinații alternative.
Americanii aleg clinici reglementate din străinătate pentru claritate, calitate și acces la programe personalizate. Ei compară adesea opțiunile din SUA cu centre care au laboratoare proprii și standarde transparente de producție.
Atunci când iau în considerare tratamentul în străinătate, pacienții se concentrează, de obicei, pe următoarele aspecte:
- Programe integrate (celule + terapii de susținere);
- Proprietate clară a procesului de producție (sursă, testare, criterii de eliberare);
- Logistică simplificată și echipe multidisciplinare;
- Informare transparentă privind eficiența terapiei cu celule stem (ce se cunoaște și ce este încă în studiu), fără promisiuni exagerate.
Unde este terapia cu celule stem ilegală — și unde o puteți obține legal în străinătate
Regulile variază mult de la o țară la alta. Unele interzic aplicațiile derivate din embrioni, altele restricționează orice producție neaprobată, iar multe clasifică produsele celulare ca medicamente de terapie avansată (ATMP), care necesită autorizare din partea agențiilor.
Să analizăm acum opțiunile disponibile pentru americanii care doresc să primească terapie cu celule stem. Iată câteva dintre cele mai comune destinații:
Este terapia cu celule stem legală în Columbia?
Expansiunea celulelor stem și protocoalele de laborator avansate sunt permise în baza reglementărilor columbiene, ceea ce face țara atractivă pentru pacienții care caută terapii cu doze mari. Totuși, supravegherea este mai redusă decât în SUA, astfel încât calitatea poate depinde mult de clinică.
Este terapia cu celule stem legală în India?
India are un cadru de reglementare formal: clonarea terapeutică este legală, în timp ce clonarea reproductivă este interzisă. Cu specialiști foarte bine pregătiți și prețuri semnificativ mai mici, India este un centru major — dar distanța mare și standardele variabile ale clinicilor pot reprezenta provocări pentru pacienții americani.
Este terapia cu celule stem legală în Caraibe (Bahamas)?
Unele clinici operează într-o „zonă gri”. Aceste tratamente sunt populare printre pacienții înstăriți, dar vin cu prețuri ridicate și puține garanții.
Este terapia cu celule stem legală în Europa?
Majoritatea terapiilor cu celule stem din Europa sunt considerate ATMP-uri. Aceasta înseamnă că necesită autorizare, iar studiile clinice și producția trebuie să respecte regulile de Bună Practică de Fabricație (GMP). Costurile sunt adesea mai mari, dar standardele sunt de încredere.
De ce Serbia devine o destinație pentru terapia cu celule stem
În Serbia, pacienții găsesc atât accesibilitate, cât și supraveghere medicală — o combinație rară în domeniul terapiilor cu celule stem. Acest echilibru este posibil deoarece țara își aliniază reglementările la standardele UE, evitând în același timp întârzierile îndelungate adesea întâlnite în Europa de Vest.
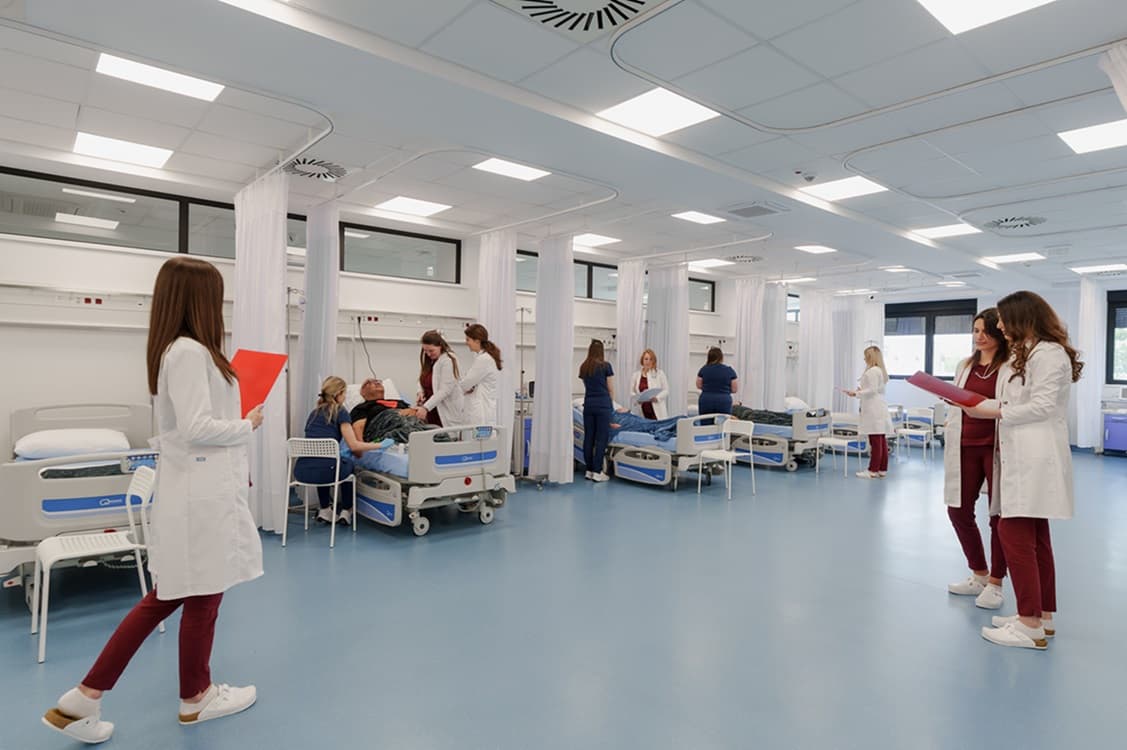
Swiss Medica este unul dintre cele mai renumite centre din regiune. Activează în domeniul medicinei regenerative și al terapiei cu celule stem încă din 2011. În 2024, clinica s-a extins semnificativ prin deschiderea unui spital ultramodern la Belgrad, cu o suprafață de 10.000 m², împărțită în cinci clădiri pe un teren de 3 hectare, devenind astfel una dintre principalele destinații pentru terapia cu celule stem din Serbia.
Spitalul nostru combină tehnologia medicală avansată cu confortul unei clinici moderne, oferind pacienților un mediu primitor în fiecare etapă a tratamentului lor.
Noua unitate a fost concepută pentru a oferi tratament sigur și personalizat la cele mai înalte standarde, cu control complet intern — de la sursa țesutului donator până la eliberarea și administrarea produsului — și monitorizare continuă după externare.
Descoperiți cum a decurs terapia cu celule stem la Swiss Medica pentru pacientul nostru din SUA.
Ghid rapid: SUA și Europa vs. Serbia — La ce se pot aștepta pacienții
| Aspect | Statele Unite | Europa | Serbia |
| Statut legal | Domeniu foarte limitat al aprobărilor federale, combinat cu variații la nivel de stat, ceea ce creează confuzie cu privire la ce terapii cu celule stem sunt legale în SUA și care sunt considerate experimentale. | Cadrul tip ATMP și aprobări riguroase, precum și excepții spitalicești sub supraveghere. | Standarde aliniate la UE; integrarea laboratorului și a actului medical sub licențe naționale. |
| Tipuri de produse aprobate | Aprobate de FDA: în principal celule stem hematopoietice pentru afecțiuni hematologice/imunitare. | Celule stem embrionare, MSC-uri. | MSC-uri adulte provenite de la donatori, opțiuni autologe în cazuri selectate; fără celule embrionare. |
| Acces | Multe indicații regenerative rămân experimentale → pacienții întreabă: „Sunt legale celulele stem în Statele Unite?” | Acces structurat prin studii/autorizații. | Acces structurat prin studii formale sau autorizații, cu criterii clare de eligibilitate și protocoale de tratament reglementate. |
| Cost | De obicei mai ridicat din cauza costurilor sistemului. | Varibil în funcție de țară/clinică. | Transparent; costuri totale ale programelor, de obicei mai reduse. |
Cum să verificați dacă o clinică funcționează legal
Folosiți această listă de verificare simplă înainte de a face o programare:
- Licențiere & domeniu: Clinica este autorizată pentru procedurile pe care le oferă? Dacă este în SUA, produsul este aprobat de FDA sau utilizat într-un studiu clinic valid/excepție corespunzătoare?
- Claritatea sursei celulare: Ce tip de celule sunt utilizate (MSC-uri de la donatori vs. autologe)? Nu ar trebui să fie folosite celule embrionare.
- Transparența producției: Celulele sunt produse într-o unitate înregistrată și auditată, cu săli sterile de nivel GMP și teste de eliberare pe lot (identitate, puritate, sterilitate, viabilitate)?
- Protocoale & dozaj: Protocolul este individualizat? Rutele de administrare și rațiunea sunt explicate clar?
- Siguranță & monitorizare: Evenimentele adverse sunt monitorizate? Există o urmărire structurată după tratament?
- Dovezi & indicații: Clinica este onestă în privința a ceea ce se cunoaște, ce rămâne în fază de cercetare și ce rezultate pot fi așteptate în mod realist?
- Consimțământ informat: Primiți documente clare privind beneficii/riscuri, alternative și costuri?
Cum să găsiți cea mai bună clinică de celule stem?
O listă a „celor mai bune clinici” ar trebui să se bazeze pe criterii, nu doar pe reclame:
- Statut de reglementare: Bază legală clară pentru fiecare produs oferit.
- Capabilități interne: Laborator integrat și criobank; control complet al procesului.
- Controale de calitate: Procese documentate la nivel GMP; certificate de lot.
- Integrare clinică: Echipe multidisciplinare, terapii de susținere (ex. fizioterapie, reabilitare țintită) și obiective realiste.
- Rezultate & transparență: Protocoale publicate acolo unde este posibil; monitorizare solidă a pacienților după tratament.
- Experiența pacientului: Accesibilitate, suport lingvistic și continuitatea îngrijirii.
Swiss Medica îndeplinește aceste criterii. Fiecare procedură cu celule stem aici respectă protocoale stricte de siguranță, utilizează preparate celulare controlate calitativ de la furnizori conformi GMP și este realizată de medici cu experiență. Această abordare oferă pacienților beneficiile unei terapii avansate, fără incertitudinile pieței nereglementate din SUA.
Pentru o imagine orientativă a costurilor tratamentului cu celule stem, majoritatea programelor variază între 7.000 € și 31.000 €*.
*Prețurile sunt orientative, bazate pe ianuarie 2025, și pot varia în funcție de gravitatea afecțiunii și de numărul de celule necesar.
Obțineți o consultație online gratuită
Faceți primul pas către recuperarea dumneavoastră.
Împărtășiți cazul echipei noastre medicale, iar noi vom pregăti un plan de tratament personalizat, adaptat nevoilor și obiectivelor dumneavoastră. Trebuie doar să completați formularul de mai jos.

Consilier medical, medic la Swiss Medica
Ce face ca Swiss Medica să fie o alegere sigură?
Siguranța pe primul loc
- Doar MSC-uri verificate din cordonul ombilical și placentă.
- Fără celule embrionare sau animale → risc mai scăzut de complicații.
- Toate celulele sunt testate intern pentru siguranță și calitate.
Îngrijire cuprinzătoare
- Multiple metode de administrare (IV, intratecal, intramuscular, local).
- Terapii regenerative suplimentare: terapie IMR, antioxidanți, fizioterapie, exosomi și secretom.
- Suport continuu: recomandări personalizate, consultații online și un control gratuit la 6 luni.
- Terapie de întreținere cu exosomi la domiciliu, cu ghid medical complet.
- Programe specializate pentru autism, în medii adaptate și prietenoase pentru copii.
Condiții unice
- Spital și laborator propriu pentru control strict al calității.
- Conformitate totală cu standardele europene.
- Echipa internațională cu experiență, care dezvoltă noi protocoale.
- Programe all-inclusive: tratament, cazare, mese, transferuri, traduceri — fără costuri ascunse.
Rezultate dovedite & încredere
- 80% dintre pacienți raportează îmbunătățiri.
- Peste 550 de mărturii video reale.
- Comunicare onestă și transparentă.
Accesibilitate & confort
- Călătorii ușoare: zboruri directe din Europa, rute accesibile din întreaga lume.
- Adaptare completă pentru mobilitate limitată.
- Sosiri/plecări flexibile, cu zile suplimentare pentru confort.
- Spații separate adaptate nevoilor pacienților.
- Familiile sunt cazate în cadrul clinicii.
Pacienții americani laudă adesea profesionalismul echipei medicale și rezultatele care le schimbă viața.
„Am venit la Swiss Medica după ce mi s-a spus că afecțiunea mea (scleroza laterală primară) era netratabilă. La doar câteva zile după terapia cu celule stem, am putut din nou să îmi ridic piciorul pentru prima dată după doi ani. Medicii, personalul și îngrijirea au fost extraordinare — această clinică mi-a redat cu adevărat speranța și calitatea vieții.”
— Pacient din SUA.
Când SUA spune „nu”, Serbia spune „bine ați venit”
Dacă vi s-a spus „nu este disponibil” sau vă este greu să navigați între regulile federale și cele de stat contradictorii, este firesc să căutați alternative. Pe măsură ce tot mai mulți pacienți continuă să întrebe dacă terapia cu celule stem este legală în SUA, Serbia oferă o opțiune transparentă, bazată pe dovezi, cu MSC-uri adulte și îngrijire cuprinzătoare.
Atunci când alegeți locația pentru tratament, siguranța, calitatea produsului și transparența legală ar trebui să fie întotdeauna priorități principale. Serbia, ca destinație, le combină pe toate, iar atunci când adăugăm și prețurile reduse, aceasta devine una dintre cele mai accesibile țări pentru tratamentul cu celule stem, raportat la valoarea obținută.
Noi credem că pacienții merită claritate deplină. Swiss Medica oferă o consultație gratuită, fără obligații, cu un specialist în medicină regenerativă. Echipa noastră are peste 14 ani de experiență și analizează cu atenție fiecare caz. Oferim îndrumare clară și împărtășim toate informațiile disponibile despre protocoale, rămânând deschiși atât în privința posibilităților, cât și a limitărilor terapiei cu celule stem.
Contact us
Faceți primul pas către o terapie cu celule stem sigură și eficientă — solicitați astăzi evaluarea medicală gratuită.
Completați formularul de mai jos și preluați controlul asupra sănătății dumneavoastră.

Consilier medical, medic la Swiss Medica
FAQ
1. Este terapia cu celule stem legală în SUA?
La nivel federal, doar un subset restrâns de terapii cu celule stem este legal în SUA — în special produsele de celule stem hematopoietice pentru afecțiuni specifice. Multe alte utilizări sunt încă în faza de investigație. Texas, Utah și Florida au creat permisiuni, dar acestea nu echivalează cu aprobarea federală.
2. De ce sunt celulele stem ilegale în Statele Unite (sau strict limitate)?
Produsele pe bază de celule stem sunt strict restricționate în SUA deoarece orice nouă terapie trebuie mai întâi să demonstreze calitatea, siguranța și eficacitatea prin studii clinice riguroase și producție conform standardelor GMP. Incidentele de siguranță din trecut au dus la o aplicare mai strictă a regulilor. Din acest motiv, cadrul legal limitează încă terapia cu celule stem în SUA la utilizări în afara aprobărilor oficiale.
3. Sunt celulele stem legale în Statele Unite pentru utilizare ortopedică sau neurologică?
Nu ca regulă generală. În SUA, terapiile cu celule stem pentru afecțiuni ortopedice sau neurologice sunt considerate, în general, investigaționale. Deși unele clinici funcționează pe baza permisiunilor la nivel de stat, acestea nu înlocuiesc legea federală. Fără aprobarea FDA, astfel de produse nu pot fi comercializate ca tratamente dovedite.
4. Este tratamentul cu celule stem legal în SUA dacă medicul meu îl oferă conform legislației statului?
Permisiunile statale nu fac automat ca un tratament cu celule stem să fie „legal” în SUA. Sfat: Verificați dacă terapia este aprobată de FDA sau dacă este oferită în cadrul unui studiu clinic înregistrat.
5. Este terapia cu celule stem legală în SUA pentru leucemie sau tulburări imune?
Da — tratamentul cu celule stem hematopoietice (formatoare de sânge) este legal în SUA și aprobat de FDA pentru indicații specifice. Alte tipuri de terapii cu celule stem nu sunt încă aprobate, ceea ce înseamnă că sunt considerate experimentale și nu pot fi oferite ca tratamente consacrate.
Lista Referințelor:
U.S. Food and Drug Administration. Human Cells, Tissues, and Cellular and Tissue-Based Products (HCT/Ps). https://www.fda.gov/vaccines-blood-biologics/cellular-gene-therapy-products/human-cells-tissues-and-cellular-and-tissue-based-products
U.S. Food and Drug Administration. Regulatory Considerations for Human Cells, Tissues, and Cellular and Tissue-Based Products: Minimal Manipulation and Homologous Use. Guidance for Industry and FDA Staff. https://www.fda.gov/media/109176/download
U.S. Food and Drug Administration. Approved Cellular and Gene Therapy Products. https://www.fda.gov/vaccines-blood-biologics/cellular-gene-therapy-products/approved-cellular-and-gene-therapy-products
U.S. Food and Drug Administration. Biologics License Applications (BLA) Process. https://www.fda.gov/vaccines-blood-biologics/licensing/biologics-license-applications-bla-process
International Society for Stem Cell Research. ISSCR Guidelines for Stem Cell Research and Clinical Translation. https://www.isscr.org/guidelines
WIRED. Florida Is Now a Haven for Unproven Stem-Cell Treatments. https://www.wired.com/story/florida-is-now-a-haven-for-unproven-stem-cell-treatments
Bioethics.com. Florida Is Now a Haven for Unproven Stem-Cell Treatments. https://bioethics.com/archives/98915
STAT News. Q&A: Bioethicist Leigh Turner on the Worrisome Boom in Unregulated Stem Cell Clinics. https://www.statnews.com/2021/11/08/bioethicist-leigh-turner-boom-unregulated-stem-cell-clinics
The Niche / IPSCELL.com. Turner Pub Charts Runaway Stem Cell Clinic Industry, FDA Needs to Think Big. https://ipscell.com/2021/11/turner-pub-charts-runaway-stem-cell-clinic-industry-fda-needs-to-think-big
MD, Pediatrician, Regenerative Medicine Specialist