Terapia komórkami macierzystymi to jedna z najbardziej obiecujących dziedzin współczesnej medycyny, jednak w Stanach Zjednoczonych pozostaje ściśle regulowana. Wielu pacjentów zadaje sobie pytanie: czy terapia komórkami macierzystymi jest legalna w USA? Krótka odpowiedź brzmi: tak — ale tylko w określonych, ograniczonych przypadkach. W tym artykule wyjaśnimy zasady, powody utrzymywania restrykcji oraz wskażemy miejsca, w których pacjenci mogą bezpiecznie podjąć leczenie za granicą.

Czym jest terapia komórkami macierzystymi?
Terapia komórkami macierzystymi wykorzystuje najsilniejsze mechanizmy naprawcze organizmu — wyspecjalizowane komórki oraz bioaktywne sygnały, które one uwalniają — aby zminimalizować stan zapalny, pobudzić regenerację i przywrócić funkcje w miejscach, gdzie medycyna konwencjonalna często okazuje się nieskuteczna.
Zamiast zastępować sprawdzone metody leczenia, takie jak operacja, farmakoterapia czy rehabilitacja, działa u ich boku, aby przyspieszyć proces zdrowienia, poprawić mobilność i podnieść jakość życia. Dla wielu pacjentów stanowi alternatywną drogę do odzyskania zdrowia w sytuacjach, gdy same tradycyjne metody nie są wystarczające.
Rodzaje komórek macierzystych stosowanych w terapii
Różne kliniki mogą korzystać z różnych źródeł komórek; w Swiss Medica używamy wyłącznie dorosłych, multipotencjalnych mezenchymalnych komórek zrębowych (MSC) oraz ich pochodnych.
- Komórki allogeniczne: komórki dawcy z pępowiny lub łożyska (pobrane po żywym porodzie). Szeroko badane pod kątem ich właściwości immunomodulacyjnych i przeciwzapalnych.
- Komórki autologiczne: własne komórki pacjenta pozyskiwane ze szpiku kostnego — lub w określonych przypadkach z tkanki tłuszczowej.
- Pochodne bezkomórkowe (np. egzosomy/sekretom): biologiczni „posłańcy”, którzy mogą być stosowani równolegle z komórkami lub jako samodzielne protokoły w łagodniejszych przypadkach.
Nie stosujemy komórek embrionalnych ani komórek iPSC.
Czy terapia komórkami macierzystymi jest legalna w USA w 2025 roku?
Tak, terapia komórkami macierzystymi jest legalna w USA, ale tylko wtedy, gdy wykorzystuje produkty zatwierdzone przez FDA w leczeniu określonych schorzeń. To właśnie zatwierdzenie przez FDA nadaje terapii status legalny na poziomie federalnym. Bez niego procedury pozostają eksperymentalne i nie mogą być oferowane jako uznane metody leczenia — nawet jeśli niektóre stany dopuszczają ich ograniczone stosowanie.
Choć nagłówki prasowe i reklamy często tworzą wrażenie szerokiego dostępu, w rzeczywistości dostępność zależy od dwóch poziomów regulacji:
- Przepisy federalne pod nadzorem Amerykańskiej Agencji ds. Żywności i Leków (FDA).
- Prawo stanowowe, które może tworzyć wyjątki, ale nie może unieważniać regulacji federalnych.
W rezultacie zakres terapii komórkami macierzystymi legalnych w USA jest w rzeczywistości znacznie węższy, niż sugerują to liczne reklamy, koncentrując się głównie na opcjach zatwierdzonych przez FDA.
Na przykład nowe przepisy stanu Floryda pozwalają licencjonowanym lekarzom (MD) i osteopatom (DO) oferować niektóre niezatwierdzone procedury komórkowe w leczeniu ran, zarządzaniu bólem i ortopedii — pod warunkiem spełnienia rygorystycznych wymogów dotyczących dokumentacji i świadomej zgody pacjenta. Podobne rozwiązania istnieją w Teksasie i Utah. Zmiany te pokazują, że krajobraz terapii komórkami macierzystymi stopniowo przesuwa się w kierunku większej dostępności dla pacjentów.
Ścieżki legalizacji przeszczepów komórek macierzystych w Stanach Zjednoczonych
Zanim jakakolwiek nowa terapia komórkami macierzystymi będzie mogła być szeroko oferowana w USA, musi przejść określone kroki prawne i regulacyjne. Aby była legalna na poziomie federalnym, każda nowa terapia komórkami macierzystymi musi przejść przez następujące etapy:
| Etap | Proces | Co to oznacza dla pacjentów |
| 1 → Specjalna kategoria (361 HCT/Ps) | Niektóre proste produkty komórkowe mogą być stosowane natychmiast, jeśli spełniają surowe zasady. | Dostępne tylko w bardzo ograniczonych przypadkach. |
| 2 → Badania kliniczne | Nowe terapie są najpierw testowane w badaniach zatwierdzonych przez FDA. | Pacjenci mogą dołączyć do badań, aby wcześniej skorzystać z terapii. |
| 3 → Dostęp w trybie „compassionate use” | W rzadkich, poważnych lub zagrażających życiu przypadkach pacjenci mogą ubiegać się o specjalne zezwolenie. | Zapewnia dostęp, gdy nie istnieją inne możliwości leczenia. |
| 4 → Pełne zatwierdzenie FDA | FDA analizuje wszystkie dane i oficjalnie zatwierdza terapię. | Leczenie staje się szeroko dostępne jako standardowa opcja w USA. |
Co FDA faktycznie dopuszcza w zakresie terapii komórkami macierzystymi w 2025 roku
FDA reguluje terapie komórkami macierzystymi głównie w ramach dwóch systemów prawnych:
| Produkt | Przykład |
| Zatwierdzone produkty komórkowe (351 HCT/Ps) Wymagają badań klinicznych, Biologics License Application (BLA) oraz produkcji zgodnej z GMP z rygorystyczną kontrolą jakości. | Przeszczepienie komórek macierzystych z krwi pępowinowej, stosowane w szpitalach w USA do odbudowy funkcji krwi i układu odpornościowego u pacjentów z białaczkami, chłoniakami i innymi poważnymi chorobami krwi (konieczna zgodność z GMP i szerokim zakresem testów). Zatwierdzone przez FDA terapie CAR-T dla określonych białaczek i chłoniaków |
| 361 HCT/Ps (mniej regulowane) Nie wymagają zatwierdzenia przed wprowadzeniem na rynek, jeśli produkt jest minimalnie przetworzony, używany do celów homologicznych i spełnia wszystkie standardy bezpieczeństwa/testów. | Filtrowanie komórek macierzystych z tkanki tłuszczowej bez zmiany ich właściwości biologicznych. Wykorzystanie komórek szpiku kostnego do produkcji krwinek (ale nie do naprawy chrząstki). |
| 351 HCT/Ps (gdy kryteria 361 nie są spełnione) Regulowane jako leki/produkty biologiczne, wymagające pełnej ścieżki: badań klinicznych i zatwierdzenia BLA. | Każdy produkt komórkowy, który jest istotnie zmodyfikowany lub stosowany do celów niehomologicznych, musi przejść pełny proces zatwierdzania FDA. |
Dlaczego terapia komórkami macierzystymi wciąż jest ograniczona w Stanach Zjednoczonych — i co to oznacza dla pacjentów
Mimo że terapia komórkami macierzystymi wykazuje ogromny potencjał na całym świecie, jej stosowanie w USA pozostaje ściśle ograniczone. Pacjenci często pytają w internecie: „Dlaczego terapia komórkami macierzystymi jest nielegalna w Stanach Zjednoczonych?” Odpowiedź leży w połączeniu debat etycznych, rygorystycznych wymogów FDA dotyczących badań klinicznych oraz trwających pytań o długoterminowe bezpieczeństwo.
Kwestie etyczne
Dyskusje wokół komórek pochodzących z embrionów doprowadziły w przeszłości do wprowadzenia surowych barier. Choć większość nowoczesnych klinik stosuje MSC (mezenchymalne komórki zrębowe), które z reguły nie budzą takich samych wątpliwości etycznych ani obaw o bezpieczeństwo jak komórki embrionalne, ustawodawcy nadal tworzą szerokie przepisy, aby uniknąć „szarych stref”.
W rezultacie niektóre terapie pozostają oficjalnie zakwalifikowane jako „nielegalne” w USA. Dzieje się tak częściowo w celu zapobiegania nadużyciom związanym z wykorzystaniem komórek embrionalnych, a także po to, by uniemożliwić klinikom oferowanie komórek przetwarzanych niezgodnie z rygorystycznymi normami FDA.
Brak badań klinicznych
Głównym ograniczeniem jest dziś poziom dowodów klinicznych wymaganych przez regulatorów. W przypadku nowych produktów komórkowych FDA żąda dużych, dobrze kontrolowanych badań. Wiele terapii, o których pacjenci czytają pod hasłem „legalne terapie komórkami macierzystymi w USA”, nie jest jeszcze w pełni zatwierdzonych, ponieważ nadal znajdują się w fazie badań.
Aby przyznać pełną aprobatę, FDA i inne instytucje wymagają długoterminowych, szeroko zakrojonych badań klinicznych, które trwają latami. Do tego czasu terapia komórkami macierzystymi pozostaje w kategorii „ograniczonej”, mimo że nowoczesne kliniki stosują już międzynarodowe standardy i technologie.
Wyzwania dotyczące skuteczności
Choć obecne dowody naukowe nie pozwalają jeszcze na ostateczne wnioski co do ogólnej skuteczności terapii komórkami macierzystymi, pacjenci na całym świecie wciąż zgłaszają znaczącą poprawę — lepszą mobilność, zmniejszenie bólu i przywrócenie funkcji.
Swiss Medica udokumentowała setki takich przypadków, z danymi z obserwacji potwierdzającymi te rezultaty. Niektóre efekty są naprawdę przełomowe:
- Samodzielne chodzenie w ciągu kilku tygodni od terapii, nawet po latach korzystania z pomocy ortopedycznych.
- Znaczące zmniejszenie przewlekłego bólu, umożliwiające przespanie całej nocy bez dyskomfortu.
- Poprawa kontroli pęcherza i innych funkcji, sięgająca w niektórych przypadkach 30–35% w ciągu kilku miesięcy.
Co to oznacza dla pacjentów
Zrozumienie ścieżek prawnych jest kluczowe dla każdego, kto rozważa terapię komórkami macierzystymi w USA.
FDA bardzo rygorystycznie reguluje te terapie, a wiele metod, które mają potwierdzony profil bezpieczeństwa za granicą, wciąż nie jest dostępnych w Stanach Zjednoczonych — wyłącznie dlatego, że nie przeszły jeszcze długotrwałego procesu zatwierdzania.
Brak zatwierdzenia przez FDA nie oznacza, że procedury te są szkodliwe. Najczęściej oznacza to po prostu, że badania nadal trwają — tak jak w przypadku każdego innowacyjnego produktu.
Co się dzieje, jeśli pacjent skorzysta z terapii w nieregulowanej klinice?
Legalne przeszczepy komórek macierzystych w ramach ścieżek dopuszczonych w Stanach Zjednoczonych (takie jak przeszczepy krwi pępowinowej w chorobach krwi) istnieją, ponieważ spełniają rygorystyczne standardy. Problem dotyczy rynku nieregulowanego: do 2021 roku badacze udokumentowali ponad 2700 klinik w USA sprzedających niezatwierdzone terapie komórkami macierzystymi. Takie placówki działają poza nadzorem FDA, opierają się na niezweryfikowanych źródłach komórek i ignorują podstawowe standardy bezpieczeństwa — co doprowadziło już do licznych ostrzeżeń FDA, a nawet procesów sądowych.
Negatywne relacje medialne często tworzą wrażenie, że wszystkie kliniki wyglądają w ten sposób. Jednocześnie FDA nie robi wystarczająco dużo, aby informować opinię publiczną o trwających badaniach, co powoduje lukę informacyjną. W rezultacie ludzie albo odrzucają potencjalnie pomocne terapie, albo mają trudności ze zrozumieniem, jak wybrać godną zaufania klinikę.
Jakie może być rozwiązanie? Choć terapie komórkami macierzystymi mogą w przyszłości uzyskać pełne zatwierdzenie FDA, już teraz kilka obiecujących metod jest dostępnych w licencjonowanych klinikach za granicą. Dla pacjentów, którzy nie chcą czekać latami na zakończenie procesu zatwierdzania w USA, przejrzysta, dobrze regulowana klinika międzynarodowa może stanowić bezpieczną i skuteczną alternatywę.
Renomowane kliniki zagraniczne działają zgodnie z surowymi regulacjami krajowymi, stosują standardy produkcji GMP oraz wykorzystują terapie, które zostały sprawdzone i zatwierdzone przez lokalne organy zdrowia — nawet jeśli wciąż oczekują na recenzję FDA.
Turystyka medyczna w zakresie terapii komórkami macierzystymi: czy to się opłaca?
W obliczu złożonych regulacji we własnym kraju wielu Amerykanów często pyta: „Dlaczego komórki macierzyste są nielegalne w Stanach Zjednoczonych w porównaniu z innymi miejscami?” To zamieszanie często skłania ich do rozważenia regulowanej turystyki medycznej, gdzie ścieżki prawne i procedury zatwierdzania są bardziej przejrzyste.
Czy podróż w celu leczenia komórkami macierzystymi jest legalna?
Każdy obywatel USA ma prawo swobodnie podróżować za granicę i podejmować niezależne decyzje dotyczące leczenia, w tym korzystania z opieki medycznej. Wynika to z konstytucyjnego prawa do wolności przemieszczania się oraz zasady świadomej zgody, która jest utrwalona w orzecznictwie amerykańskim.
Jednak w niektórych krajach, gdzie terapia komórkami macierzystymi jest legalna, przepisy równoważne tym z USA nie obowiązują. Pacjenci mogą uzyskać dostęp do terapii szybciej, ale przy mniejszym nadzorze — dlatego weryfikacja kliniki jest kluczowa.
Co pacjent powinien sprawdzić przed przyjazdem do kliniki?
- Regulacje w kraju docelowym — upewnij się, że terapia, której szukasz, jest legalna i oficjalnie regulowana.
- Wiarygodność kliniki — sprawdź, czy klinika posiada licencję, historię medyczną i czy przestrzega lokalnych standardów opieki zdrowotnej.
Dlaczego wielu Amerykanów wybiera terapię komórkami macierzystymi za granicą?
Dla pacjentów, którzy nie chcą czekać latami na zatwierdzenie FDA, pojawiają się alternatywne kierunki leczenia.
Amerykanie wybierają regulowane kliniki zagraniczne ze względu na przejrzystość, jakość i dostęp do spersonalizowanych programów. Często porównują dostępne opcje w USA z ośrodkami, które dysponują własnymi laboratoriami i transparentnymi standardami produkcji.
Przy wyborze leczenia za granicą pacjenci zazwyczaj zwracają uwagę na następujące aspekty:
- Zintegrowane programy (komórki + terapie wspomagające).
- Przejrzystość w zakresie produkcji (pochodzenie, testowanie, kryteria dopuszczenia).
- Uproszczona logistyka i zespoły multidyscyplinarne.
- Transparentna edukacja na temat skuteczności terapii komórkami macierzystymi (co już wiadomo, a co nadal jest badane), bez obietnic wykraczających poza dowody naukowe.
Gdzie terapia komórkami macierzystymi jest nielegalna — a gdzie można legalnie skorzystać z niej za granicą
Przepisy różnią się znacznie w zależności od kraju. Niektóre zakazują stosowania komórek pochodzących z embrionów, inne ograniczają wszelką niezatwierdzoną produkcję, a wiele klasyfikuje produkty komórkowe jako zaawansowane produkty lecznicze terapii (ATMP), które wymagają zgody odpowiednich agencji.
Przyjrzyjmy się teraz opcjom dostępnym dla Amerykanów, którzy chcą poddać się terapii komórkami macierzystymi. Oto niektóre z najczęściej wybieranych kierunków:
Czy terapia komórkami macierzystymi jest legalna w Kolumbii?
Ekspansja komórek i zaawansowane protokoły laboratoryjne są dozwolone w ramach kolumbijskich regulacji, co sprawia, że kraj ten przyciąga pacjentów poszukujących terapii wysokimi dawkami. Nadzór jest jednak słabszy niż w USA, dlatego jakość zależy w dużej mierze od konkretnej kliniki.
Czy terapia komórkami macierzystymi jest legalna w Indiach?
Indie mają formalne ramy regulacyjne: klonowanie terapeutyczne jest legalne, natomiast klonowanie reprodukcyjne jest zakazane. Dzięki wysoko wykwalifikowanym specjalistom i znacznie niższym cenom, kraj ten stanowi ważne centrum terapii — choć dla pacjentów z USA wyzwaniem mogą być długie podróże i zróżnicowany poziom klinik.
Czy terapia komórkami macierzystymi jest legalna na Karaibach (Bahamy)?
Niektóre kliniki działają w swoistej „szarej strefie”. Terapie te cieszą się popularnością wśród zamożnych pacjentów, ale wiążą się z wysokimi kosztami i ograniczonymi gwarancjami.
Czy terapia komórkami macierzystymi jest legalna w Europie?
Większość terapii komórkami macierzystymi w Europie jest klasyfikowana jako ATMP. Oznacza to, że wymagają one autoryzacji, a badania kliniczne i produkcja muszą być prowadzone zgodnie z zasadami Good Manufacturing Practice (GMP). Koszty są często wyższe, ale standardy pozostają wiarygodne.
Dlaczego Serbia staje się kierunkiem terapii komórkami macierzystymi
W Serbii pacjenci znajdują zarówno dostępność, jak i nadzór medyczny — rzadkie połączenie w dziedzinie terapii komórkami macierzystymi. Ta równowaga jest możliwa dzięki temu, że kraj dostosowuje swoje regulacje do standardów UE, jednocześnie unikając długich opóźnień, które często występują w Europie Zachodniej.
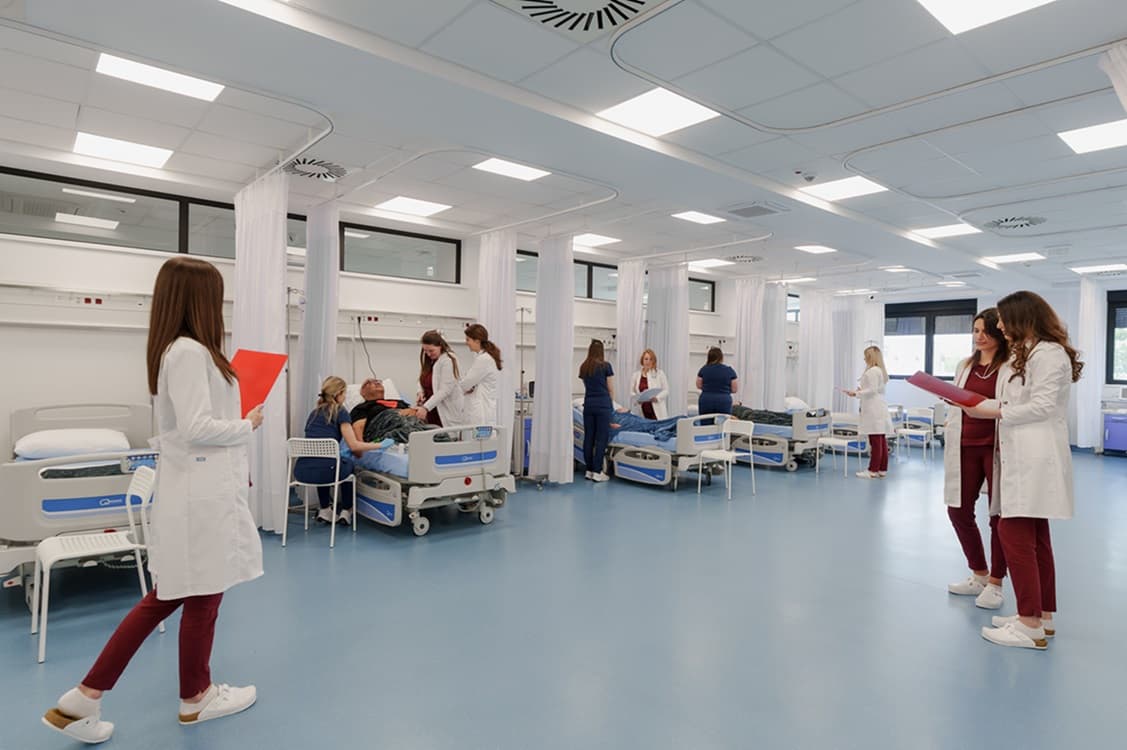
Swiss Medica jest jednym z najbardziej renomowanych ośrodków w regionie. Klinika działa w obszarze medycyny regeneracyjnej i terapii komórkami macierzystymi od 2011 roku. W 2024 roku placówka znacząco się rozwinęła, otwierając nowoczesny szpital w Belgradzie o powierzchni 10 000 m², obejmujący pięć budynków na terenie o powierzchni 3 hektarów, co czyni go jednym z wiodących miejsc terapii komórkami macierzystymi w Serbii.
Nasz szpital łączy zaawansowaną technologię medyczną z komfortem nowoczesnej kliniki, oferując pacjentom przyjazne otoczenie na każdym etapie leczenia.
Nowy obiekt został zaprojektowany tak, aby zapewniać bezpieczną, spersonalizowaną terapię na najwyższym poziomie, z pełną kontrolą wewnętrzną — od pozyskania tkanek dawcy, przez proces wytwarzania i dopuszczenie produktu, aż po jego zastosowanie — oraz z ciągłą opieką po wypisie.
Zobacz, jak wyglądała terapia komórkami macierzystymi w Swiss Medica u naszego pacjenta ze Stanów Zjednoczonych.
Krótki przewodnik: USA i Europa vs. Serbia — czego mogą oczekiwać pacjenci
| Aspekt | Stany Zjednoczone | Europa | Serbia |
| Status prawny | Wąski zakres federalnych zatwierdzeń w połączeniu z różnicami na poziomie stanowym powoduje dezorientację, które terapie komórkami macierzystymi są w USA legalne, a które eksperymentalne. | Ramy w stylu ATMP i rygorystyczne zatwierdzenia, a także wyjątki szpitalne pod ścisłym nadzorem. | Standardy zgodne z UE; zintegrowane laboratorium i opieka kliniczna w ramach krajowych licencji. |
| Rodzaje zatwierdzonych produktów | Zatwierdzone przez FDA: głównie krwiotwórcze komórki macierzyste w chorobach hematologicznych i immunologicznych. | Komórki embrionalne, MSC. | Dorosłe allogeniczne MSC, opcje autologiczne w wybranych przypadkach; brak komórek embrionalnych. |
| Dostęp | Wiele wskazań regeneracyjnych pozostaje w fazie badań → pacjenci pytają: czy komórki macierzyste są legalne w USA? | Ustrukturyzowany dostęp poprzez badania/zezwolenia. | Ustrukturyzowany poprzez formalne badania lub zezwolenia, z określonymi kryteriami kwalifikacji i regulowanymi protokołami leczenia. |
| Koszt | Często wyższy z powodu kosztów systemowych. | Zależy od kraju/kliniki. | Przejrzyste zasady; zazwyczaj niższe całkowite koszty programu. |
Jak zweryfikować, czy klinika działa legalnie
Skorzystaj z tej prostej checklisty przed rezerwacją:
- Licencje i zakres działalności: Czy klinika posiada licencję na procedury, które oferuje? Jeśli znajduje się w USA — czy produkt jest zatwierdzony przez FDA albo stosowany w ramach ważnego badania klinicznego/właściwego wyjątku?
- Źródło komórek: Jakie komórki są używane (allogeniczne MSC czy autologiczne)? Nie powinny być stosowane komórki embrionalne.
- Przejrzystość procesu produkcji: Czy komórki są wytwarzane w zarejestrowanym, audytowanym laboratorium z czystymi pomieszczeniami klasy GMP i testami każdej serii (tożsamość, czystość, sterylność, żywotność)?
- Protokoły i dawkowanie: Czy protokół jest indywidualizowany? Czy drogi podania i ich uzasadnienie są jasno wyjaśnione?
- Historia bezpieczeństwa i opieka po terapii: Czy klinika monitoruje działania niepożądane? Czy istnieje strukturalny system obserwacji po leczeniu?
- Dowody i wskazania: Czy klinika uczciwie przedstawia, co jest już potwierdzone, co nadal pozostaje w fazie badań i jakich efektów można rozsądnie oczekiwać?
Jak znaleźć najlepszą klinikę terapii komórkami macierzystymi?
Lista „najlepszych klinik” powinna być tworzona w oparciu o kryteria, a nie reklamy:
- Status regulacyjny: Jasna podstawa prawna dla każdego oferowanego produktu.
- Możliwości wewnętrzne: Zintegrowane laboratorium i kriobank; pełna kontrola procesu.
- Kontrola jakości: Udokumentowane procesy zgodne z GMP; certyfikaty serii.
- Integracja kliniczna: Zespoły multidyscyplinarne, terapie wspomagające (np. fizjoterapia, ukierunkowana rehabilitacja) oraz realistyczne cele.
- Wyniki i przejrzystość: Publikowane protokoły, jeśli to możliwe; solidna obserwacja pacjentów po leczeniu.
- Doświadczenie pacjenta: Dostępność, wsparcie językowe i ciągłość opieki.
Swiss Medica spełnia te kryteria. Każda procedura z użyciem komórek macierzystych realizowana jest tutaj zgodnie z rygorystycznymi protokołami bezpieczeństwa, z wykorzystaniem preparatów komórkowych kontrolowanej jakości od dostawców zgodnych z GMP, a także z udziałem doświadczonych lekarzy. Takie podejście zapewnia pacjentom korzyści z zaawansowanej terapii, bez niepewności związanej z nieregulowanym rynkiem w USA.
Dla orientacyjnego przeglądu kosztów terapii komórkami macierzystymi — większość programów mieści się w przedziale 7 000–31 000 €*.
*Ceny są orientacyjne, oparte na danych ze stycznia 2025 roku i mogą się różnić w zależności od stopnia zaawansowania schorzenia oraz wymaganej liczby komórek.
Uzyskaj bezpłatną konsultację online
Zrób pierwszy krok w stronę zdrowia.
Podziel się swoim przypadkiem z naszym zespołem medycznym, a przygotujemy spersonalizowany plan leczenia dostosowany do Twoich potrzeb i celów. Wystarczy, że wypełnisz poniższy formularz.

Doradca medyczny, lekarz Swiss Medica
Dlaczego Swiss Medica to bezpieczny wybór?
Bezpieczeństwo przede wszystkim
- Wyłącznie zweryfikowane MSC z pępowiny i łożyska.
- Brak komórek embrionalnych i zwierzęcych → mniejsze ryzyko powikłań.
- Wszystkie komórki testowane są wewnętrznie pod kątem bezpieczeństwa i jakości.
Kompleksowa opieka
- Różne metody podania (dożylne, dokanałowe, domięśniowe, miejscowe).
- Terapie wspomagające regenerację: IMR, antyoksydanty, fizjoterapia, egzosomy i sekretom.
- Ciągłe wsparcie: indywidualne zalecenia, konsultacje online oraz darmowa kontrola po 6 miesiącach.
- Terapia podtrzymująca egzosomami w domu z pełnym przewodnikiem medycznym.
- Specjalistyczne programy dla dzieci z autyzmem w dostosowanym, przyjaznym środowisku.
Unikalne warunki
- Własny szpital i laboratorium zapewniające ścisłą kontrolę jakości.
- Pełna zgodność ze standardami europejskimi.
- Doświadczony, międzynarodowy zespół opracowujący nowe protokoły.
- Programy „all-inclusive”: leczenie, pobyt, wyżywienie, transfery, tłumaczenia — bez ukrytych kosztów.
Udowodnione efekty i zaufanie
- 80% pacjentów zgłasza poprawę.
- Ponad 550 autentycznych wideoreferencji.
- Uczciwa, przejrzysta komunikacja.
Dostępność i komfort
- Łatwy dojazd: bezpośrednie loty z Europy, korzystne cenowo połączenia z całego świata.
- Pełne dostosowanie dla osób o ograniczonej mobilności.
- Elastyczne terminy przyjazdu/wyjazdu, z możliwością dodatkowych dni dla komfortu.
- Oddzielne przestrzenie dostosowane do potrzeb pacjentów.
- Zakwaterowanie rodzin w obrębie kliniki.
Amerykańscy pacjenci często chwalą profesjonalizm zespołu medycznego oraz przełomowe rezultaty terapii.
“Przyjechałem do Swiss Medica po tym, jak powiedziano mi, że moja choroba (pierwotne stwardnienie boczne – Primary Lateral Sclerosis) jest nieuleczalna. Już po kilku dniach terapii komórkami macierzystymi mogłem ponownie podnieść nogę — po raz pierwszy od dwóch lat. Lekarze, personel i opieka byli znakomici — ta klinika naprawdę przywróciła mi nadzieję i jakość życia.”
— Pacjent ze Stanów Zjednoczonych
Gdy USA mówi „nie”, Serbia mówi „zapraszamy”
Jeśli usłyszałeś „niedostępne” lub masz trudności z poruszaniem się po sprzecznych przepisach federalnych i stanowowych, naturalne jest, że zaczynasz szukać innych możliwości. Ponieważ wielu pacjentów wciąż pyta, czy terapia komórkami macierzystymi jest legalna w USA, Serbia oferuje przejrzystą, opartą na dowodach opcję z wykorzystaniem dorosłych MSC i kompleksowej opieki.
Przy wyborze miejsca leczenia bezpieczeństwo, jakość preparatów oraz przejrzystość prawna powinny zawsze być priorytetem. Serbia łączy te elementy, a w połączeniu z korzystnymi cenami sprawia, że jest jednym z najtańszych krajów pod względem stosunku jakości do kosztów w terapii komórkami macierzystymi.
Wierzymy, że pacjenci zasługują na pełną jasność. Swiss Medica oferuje bezpłatną, niezobowiązującą konsultację ze specjalistą medycyny regeneracyjnej. Nasz zespół ma ponad 14 lat doświadczenia i dokładnie analizuje każdy przypadek. Udzielamy jasnych wskazówek, dzielimy się wszystkimi dostępnymi informacjami na temat protokołów i pozostajemy otwarci zarówno na możliwości, jak i ograniczenia terapii komórkami macierzystymi.
Skontaktuj się z nami
Zrób pierwszy krok w stronę bezpiecznej i skutecznej terapii komórkami macierzystymi — zamów swoją bezpłatną ocenę medyczną już dziś. Wypełnij poniższy formularz i przejmij kontrolę nad swoim zdrowiem.

Doradca medyczny, lekarz Swiss Medica
FAQ
1. Czy terapia komórkami macierzystymi jest legalna w USA?
Na poziomie federalnym tylko niewielka część terapii komórkami macierzystymi jest legalna w USA — w szczególności produkty krwiotwórczych komórek macierzystych stosowane w określonych schorzeniach. Wiele innych zastosowań wciąż pozostaje w fazie badań. Teksas, Utah i Floryda wprowadziły własne zezwolenia, ale nie są one równoznaczne z aprobatą federalną.
2. Dlaczego komórki macierzyste są w USA nielegalne (lub tak ściśle ograniczone)?
Produkty komórkowe są w USA rygorystycznie ograniczone, ponieważ każda nowa terapia musi najpierw wykazać jakość, bezpieczeństwo i skuteczność poprzez rygorystyczne badania kliniczne oraz produkcję zgodną ze standardami GMP. Dawne incydenty dotyczące bezpieczeństwa doprowadziły do zaostrzenia egzekwowania prawa. Dlatego obecne regulacje ograniczają stosowanie terapii komórkami macierzystymi w USA poza zatwierdzonymi wskazaniami.
3. Czy komórki macierzyste są legalne w USA w zastosowaniach ortopedycznych lub neurologicznych?
Nie jako zasada ogólna. W USA terapie komórkami macierzystymi w ortopedii czy neurologii są generalnie traktowane jako eksperymentalne. Niektóre kliniki działają na podstawie zezwoleń stanowowych, ale te nie uchylają prawa federalnego. Bez zatwierdzenia FDA takie produkty nie mogą być oferowane jako sprawdzone terapie.
4. Czy leczenie komórkami macierzystymi w USA jest legalne, jeśli mój lekarz oferuje je na podstawie prawa stanowowego?
Zezwolenia stanowowe nie oznaczają automatycznie, że dana terapia komórkami macierzystymi jest „legalna” w USA. Wskazówka: sprawdź, czy terapia jest zatwierdzona przez FDA lub czy jest oferowana w ramach zarejestrowanego badania klinicznego.
5. Czy terapia komórkami macierzystymi jest legalna w USA w leczeniu białaczki lub zaburzeń immunologicznych?
Tak — terapia krwiotwórczymi (hematopoetycznymi) komórkami macierzystymi jest legalna w USA i zatwierdzona przez FDA w określonych wskazaniach. Inne rodzaje terapii komórkami macierzystymi wciąż pozostają niezatwierdzone, co oznacza, że są traktowane jako eksperymentalne i nie mogą być oferowane jako standardowe leczenie.
Źródła:
U.S. Food and Drug Administration. Human Cells, Tissues, and Cellular and Tissue-Based Products (HCT/Ps). https://www.fda.gov/vaccines-blood-biologics/cellular-gene-therapy-products/human-cells-tissues-and-cellular-and-tissue-based-products
U.S. Food and Drug Administration. Regulatory Considerations for Human Cells, Tissues, and Cellular and Tissue-Based Products: Minimal Manipulation and Homologous Use. Guidance for Industry and FDA Staff. https://www.fda.gov/media/109176/download
U.S. Food and Drug Administration. Approved Cellular and Gene Therapy Products. https://www.fda.gov/vaccines-blood-biologics/cellular-gene-therapy-products/approved-cellular-and-gene-therapy-products
U.S. Food and Drug Administration. Biologics License Applications (BLA) Process. https://www.fda.gov/vaccines-blood-biologics/licensing/biologics-license-applications-bla-process
International Society for Stem Cell Research. ISSCR Guidelines for Stem Cell Research and Clinical Translation. https://www.isscr.org/guidelines
WIRED. Florida Is Now a Haven for Unproven Stem-Cell Treatments. https://www.wired.com/story/florida-is-now-a-haven-for-unproven-stem-cell-treatments
Bioethics.com. Florida Is Now a Haven for Unproven Stem-Cell Treatments. https://bioethics.com/archives/98915
STAT News. Q&A: Bioethicist Leigh Turner on the Worrisome Boom in Unregulated Stem Cell Clinics. https://www.statnews.com/2021/11/08/bioethicist-leigh-turner-boom-unregulated-stem-cell-clinics
The Niche / IPSCELL.com. Turner Pub Charts Runaway Stem Cell Clinic Industry, FDA Needs to Think Big. https://ipscell.com/2021/11/turner-pub-charts-runaway-stem-cell-clinic-industry-fda-needs-to-think-big
MD, Pediatrician, Regenerative Medicine Specialist