Avec l’augmentation du nombre de personnes ayant subi une nouvelle infection à coronavirus (le soi-disant COVID-19 ou SRAS-nCOV2), les informations semblent indiquer que, loin de tous les cas, la maladie passe sans laisser de trace. En particulier, la Hong Kong’s Hospital Authority a publié un communiqué selon lequel, sur les 12 patients suivis après une infection au COVID-19, 3 présentaient des signes de diminution marquée de la fonction pulmonaire: essoufflement en marchant plus vite; selon le Dr Tsang, la diminution de la fonction pulmonaire chez ces patients atteint 20-30%. Actuellement, les patients subissent un examen supplémentaire. Selon des données préliminaires, la tomodensitométrie des patients de l’hôpital Princess Margaret révèle des changements dans les poumons par le type de verre dépoli, ce qui indique des dommages aux organes. Nous sommes convaincus que dans un avenir proche, des informations plus détaillées apparaîtront sur les patients décrits, ainsi que sur d’autres patients qui se sont rétablis après une pneumonie associée au COVID-19. En outre, le Dr Tsang prévoit de surveiller les effets indésirables à long terme chez les patients en convalescence, tels que la formation de fibrose pulmonaire.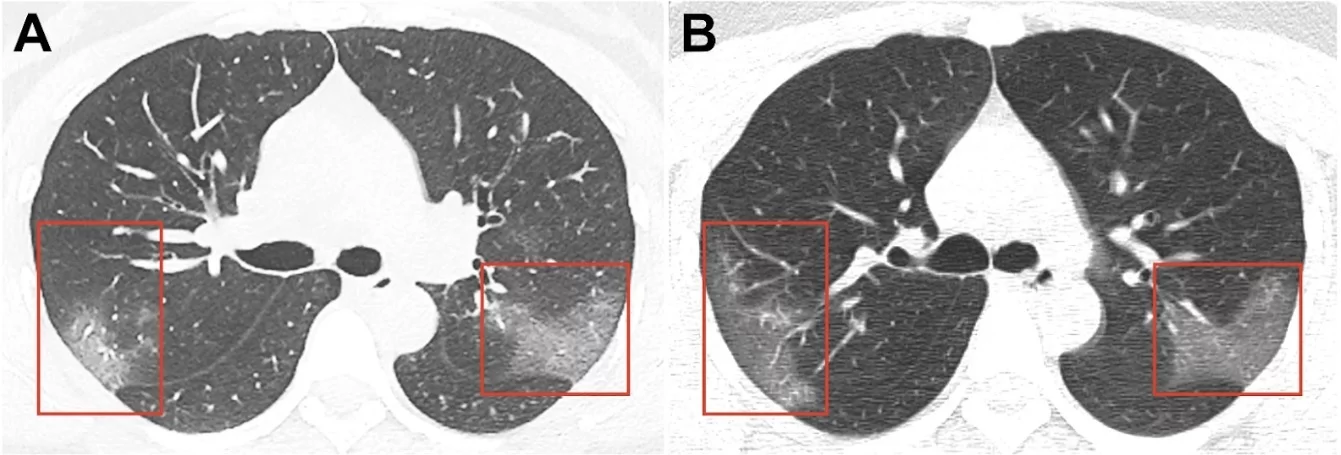
Comment les CSM peuvent-ils aider dans cette situation?
Lors de lésions pulmonaires chroniques ou aiguës, une réponse immunitaire inadéquate et des processus de récupération (réparation) altérés peuvent provoquer des lésions irréversibles du tissu pulmonaire, ce qui conduit à la formation de fibrose et à une diminution de la fonction pulmonaire. En conséquence, une recherche active est en cours pour de nouvelles stratégies thérapeutiques visant à réduire l’inflammation actuelle et, en même temps, à stimuler la régénération des cellules des alvéoles endommagées. Les cellules souches mésenchymateuses (CSM) sont capables de moduler la reproduction, l’activation et la fonction effectrice de toutes les cellules du système immunitaire, qui jouent un rôle important dans la pathogenèse des maladies pulmonaires aiguës et chroniques. En plus de réduire le potentiel pro-inflammatoire des alvéoles pulmonaires infiltrant les cellules immunitaires, les CSM peuvent stimuler la réparation des tissus endommagés par des mécanismes paracrines (en utilisant des molécules de signalisation).
CSM et syndrome de détresse respiratoire aiguë (SDRA, anglais – SRAS)
Actuellement, les résultats de la première étude pilote sur l’utilisation de la perfusion intraveineuse de CSM du cordon ombilical chez des patients atteints de pneumonie causée par COVID-19, qui a été menée à l’hôpital YouAn de Pékin en janvier-février 2020, sont actuellement publiés. Sur les 7 patients inclus dans cette étude, cinq présentaient de graves fuites. Les résultats de cette première et petite étude sont encourageants: au jour 2 après l’administration intraveineuse de CSM, tous les patients ont montré une amélioration des performances respiratoires (fonction pulmonaire) et d’autres symptômes de la maladie, puis tous les patients sont entrés dans la phase de convalescence.
Parmi les mécanismes potentiels de cette amélioration, les auteurs suggèrent une diminution du nombre de cellules CXCR3 + CD4 + T hyperactivées productrices de cytokines, de cellules T CXCR3 + CD8 + et de cellules CXCR3 + NK, qui provoquent le phénomène de la «tempête des cytokines» et peuvent entraîner une complication grave de l’infection à coronavirus – respiratoire aiguë syndrome de détresse (SDRA, anglais – SRAS) – la principale cause de décès des patients atteints de COVID-19.
Cette hypothèse est confirmée par le fait que l’administration intraveineuse de CSM a entraîné une diminution significative de la concentration de la cytokine pro-inflammatoire clé, le TNF-a, et une augmentation de la teneur en facteur anti-inflammatoire IL-10. De plus, les auteurs ont observé une augmentation de la population de cellules dendritiques anti-inflammatoires CD14 + CD11c + CD11bmid, limitant également l’intensité de l’inflammation dans les poumons.
Il convient de noter que l’administration intraveineuse est la plus efficace dans le traitement des maladies pulmonaires, car toutes les cellules introduites pénètrent dans le cœur droit par le flux sanguin, et de là dans l’artère pulmonaire, et dans l’heure qui suit la perfusion, la grande majorité des CSM injectées sont concentrées dans le parenchyme pulmonaire.
Bien sûr, il est nécessaire de poursuivre les recherches sur le potentiel de la thérapie cellulaire chez les patients atteints de COVID-19 – chez un plus grand nombre de patients, plusieurs études dans ce sens ont été annoncées [6].
Des études précliniques récemment publiées ont apporté un éclairage supplémentaire sur le rôle des CSM dans la thérapie ARDS. Ainsi, les CSM via des mécanismes dépendants de la PGE et de l’IL10 réduisent l’accumulation de neutrophiles dans les poumons et la production de TNF-a dans le SDRA provoquée par l’introduction du lipopolysaccharide d’Escherichia coli. Il a également été démontré que la production de cellules souches du facteur de croissance des kératinocytes (KGF), du facteur de croissance endothélial vasculaire (VEGF) et du facteur de croissance des hépatocytes (HGF) stimule la régénération des alvéolocytes de type II, prévient la mort des cellules endothéliales vasculaires et restaure la barrière endothéliale alvéolaire endommagée dans les poumons ARDS? Ce qui entraîne une diminution de l’œdème local, une meilleure oxygénation et survie.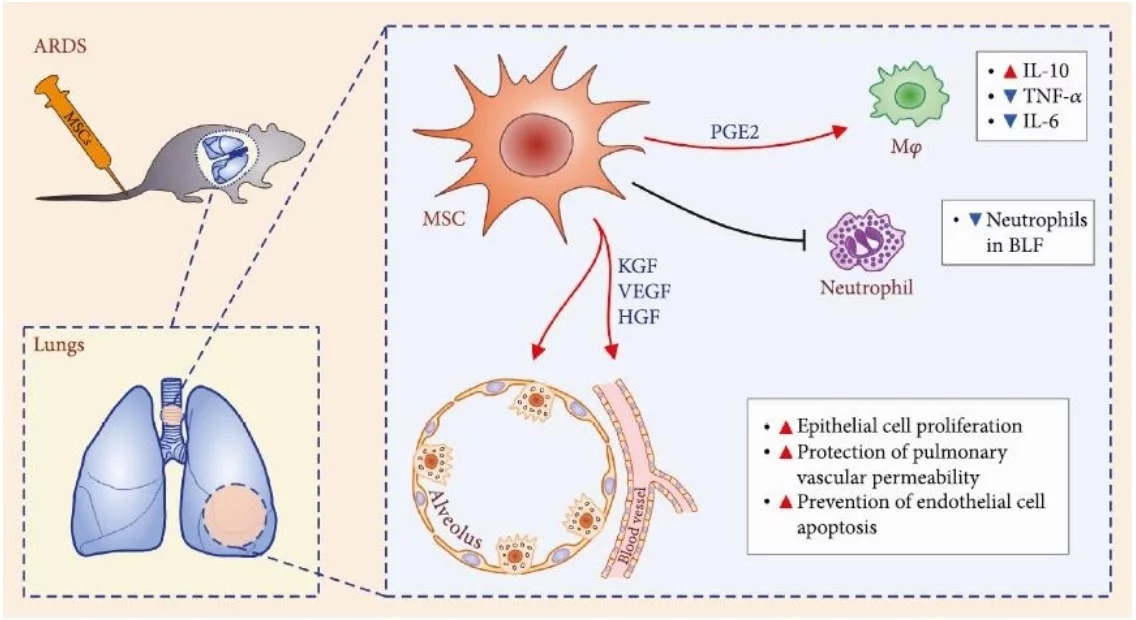
Les effets de l’administration intraveineuse de CSM de la moelle osseuse chez l’homme atteint de SDRA ont également été étudiés par Wilson et d’autres. Il a été démontré que l’introduction de CSM à des doses de 1,5 et 10 millions / kg de poids corporel était sûre et bien tolérée par les patients, les résultats étaient également optimistes et ont conduit à l’organisation d’une étude plus vaste dont les résultats n’ont pas encore été publiés.
Ainsi le réseau de données accumulées permet de classer l’administration interne des cellules souches mésenchymateuses comme l’une des méthodes de traitement ARDS prometteuses associées à la maladie COVID-19.
CSM dans le traitement de la fibrose pulmonaire chez les convalescents COVID-19
Cependant le nombre de cas de fibrose pulmonaire post-inflammatoire sévère augmentera avec le nombre de patients qui ont réussi à faire face à une pneumonie bilatérale causée par COVID-19 : les phénomènes signalés par le Dr Tsang et la Hong Kong’s Hospital Authority.
Actuellement il n’y a pas de données provenant d’études pilotes sur les effets de l’utilisation de cellules souches mésenchymateuses dans cette catégorie de patients. Cependant une étude du rôle des CSM dans le traitement d’autres affections associées au remplacement pulmonaire par du tissu fibreux (conjonctif, cicatriciel) nous permet d’espérer avec optimisme des résultats officiels.
Des études précliniques sur un modèle de maladie pulmonaire obstructive chronique (MPOC), dont l’une des principales manifestations est la fibrose et l’emphysème, ont montré que les macrophages sont l’une des principales cibles des CSM transplantées: les cellules souches ont augmenté le contenu de la fraction anti-inflammatoire des macrophages M2 et ont diminué le contenu des cellules M1 pro-inflammatoires et ont également réduit la concentration des métalloprotéinases matricielles MMP-2, MMP-9 et MMP-12, inhibant ainsi la dégradation du squelette d’élastine des poumons et le développement de la fibrose.
En conséquence la gravité des changements emphysémateux a diminué, le taux de perte d’alvéoles fonctionnelles a également diminué et des indicateurs de ventilation tels que la capacité vitale des poumons et le débit expiratoire forcé se sont améliorés.. Dans ce cas le mécanisme d’exposition à prédominance paracrine est confirmé par le fait que l’environnement CSM conditionné possède également les propriétés positives énumérées.
Les effets positifs des CSM dans la BPCO sont également associés à l’inhibition de l’apoptose, c’est-à-dire la mort programmée des alvéolocytes de type II (ATII) par une expression accrue du gène Bcl-2 et l’inhibition de la cascade des caspases, un médiateur clé de l’apoptose.
Les CSM peuvent empêcher le développement de la fibrose pulmonaire causée par les radiations. La diminution des dommages inflammatoires au tissu pulmonaire dans cette étude était corrélée à une diminution de la production de cytokines, une diminution de la prolifération des fibroblastes et une accumulation de collagène.
De la même manière l’administration intraveineuse de CSM protège également contre la fibrose pulmonaire causée par la toxine de bléomycine: la thérapie par cellules souches a montré une diminution de l’inflammation dans les alvéoles, une diminution de l’activité des principaux déclencheurs de la fibrose – -2, MMP-9 et MMP-13, et aussi, le plus important, – amélioration de la structure pulmonaire et augmentation de la survie des animaux de laboratoire.
Il est à noter que les principaux effets antifibrotiques des CSM se produisent principalement au stade de la formation du tissu cicatriciel et sont médiés par des effets sur les mécanismes de l’inflammation et de la mort cellulaire, ainsi que sur la stimulation de la régénération des cellules des alvéoles endommagées. Ceci posé nous supposons que l’effet préventif maximal chez les patients souffrant de pneumonie et de SDRA provoquée par une infection à coronavirus COVID-19 devrait être attendu pendant le traitement dans les 5 mois après la maladie.
ConclusionEn résumant ce qui précède, nous pouvons tirer les conclusions suivantes:
- le traitement par cellules souches mésenchymateuses s’est révélé efficace dans le développement de la pneumonie et du syndrome de détresse respiratoire aiguë (SDRA, SRAS), y compris celui causé par le coronavirus COVID-19;
- la thérapie par les cellules souches mésenchymateuses est une voie prometteuse dans la prévention du développement de la fibrose pulmonaire post-inflammatoire chez les patients après avoir subi une pneumonie associée au COVID-19;
- le moment optimal pour ce type de thérapie est jusqu’à 4-5 mois après la maladie;
- le traitement par cellules souches mésenchymateuses chez les patients atteints de maladies pulmonaires est toléré de manière satisfaisante et ne provoque pas le développement d’effets secondaires.
MD, Pediatrician, Regenerative Medicine Specialist