Le trouble du spectre de l’autisme (TSA) est un trouble neurodéveloppemental complexe sans origine unique clairement identifiable. Les recherches actuelles montrent que les causes du TSA résultent d’une interaction complexe entre la prédisposition génétique, les influences environnementales prénatales et les processus cellulaires précoces qui façonnent le développement du cerveau. Plutôt que d’identifier une cause principale de l’autisme, la science reconnaît de plus en plus l’autisme comme le résultat de facteurs biologiques combinés agissant pendant les stades critiques du neurodéveloppement.
Dans cet article, nous explorons les causes de l’autisme chez les enfants d’un point de vue biologique et développemental. Comprendre les mécanismes sous-jacents permet aux familles de s’éloigner des approches culpabilisantes aujourd’hui dépassées et de s’orienter vers des stratégies proactives et fondées sur des preuves qui répondent aux besoins neurologiques et physiologiques spécifiques des enfants.
Pourquoi les causes de l’autisme sont-elles si complexes ?
Des décennies de recherche sur l’autisme et ses causes suggèrent qu’il n’y a pas d’origine unique à ce trouble, et le réduire à une seule constitue une simplification excessive. Le développement du cerveau humain implique des milliards de neurones et des milliers de milliards de connexions, et toute variation de ce processus est rarement le résultat d’un événement unique.

L’autisme comme spectre et non comme un trouble unique
Parce que le TSA se manifeste différemment chez chaque individu, les causes de l’autisme (Asperger et autres formes incluses) sont probablement tout aussi diverses. Le terme « spectre » ne renvoie pas uniquement aux symptômes, mais aussi aux mécanismes biologiques qui y conduisent. Deux enfants ayant le même diagnostic peuvent présenter des profils génétiques ou des marqueurs biologiques totalement différents, faisant de l’autisme un terme générique qui englobe de multiples trajectoires de développement.
Autisme : raisons pour lesquelles les explications simples sont insuffisantes
Les tentatives visant à identifier un « déclencheur » unique de l’autisme ont systématiquement échoué, car le développement du cerveau est influencé par un grand nombre de facteurs. Plutôt qu’une cause unique de l’autisme, les chercheurs analysent comment différents facteurs génétiques et environnementaux interagissent jusqu’à atteindre un certain seuil. Une fois ce seuil franchi, les schémas de connectivité cérébrale commencent à s’écarter des trajectoires neurotypiques, ce qui conduit aux caractéristiques sociales et sensorielles du TSA.
Génétique : un facteur majeur parmi l’autisme et ses causes ?
Dans la majorité des cas, la cause est en partie liée au code génétique. Cependant, cela ne signifie pas qu’il existe un « gène de l’autisme » unique. Il s’agit plutôt d’un ensemble complexe de variations, à la fois héritées et spontanées, qui influencent la manière dont les neurones communiquent.
Mutations génétiques rares et variantes génétiques courantes
La recherche distingue les mutations « de novo » – des modifications spontanées de l’ADN non héritées des parents – des variantes génétiques courantes présentes dans la population générale. Si certaines mutations rares peuvent avoir un impact important sur le développement, c’est le plus souvent l’effet cumulatif de nombreuses variantes qui constitue un facteur majeur dans la susceptibilité à l’autisme. Ces variations agissent comme un « bruit de fond » pouvant rendre le cerveau en développement plus sensible aux facteurs de stress externes.
Autisme : raisons pour lesquelles l’autisme présente un caractère familial
Les études menées sur des jumeaux et des fratries montrent que la cause de l’autisme est fréquemment liée à un terrain génétique partagé au sein d’une même famille. Ainsi, lorsqu’un enfant est diagnostiqué avec un TSA, la probabilité est plus élevée pour ses frères et sœurs. L’autisme et ses causes possibles doivent donc être compris comme le résultat d’interactions complexes entre facteurs héréditaires et influences environnementales, encore en cours d’étude.
Le rôle de l’épigénétique : interaction entre les gènes et l’environnement
L’épigénétique étudie les mécanismes moléculaires qui régulent l’expression des gènes sans modifier la séquence de l’ADN. Des facteurs environnementaux et physiologiques peuvent influencer ces mécanismes. Contrairement aux mutations génétiques, ces processus modulent la manière dont l’information génétique est utilisée par l’organisme, sans en altérer la structure. Ce domaine est essentiel, car il permet d’expliquer comment la prédisposition génétique, les influences environnementales et les mécanismes biologiques interagissent au cours du développement.
Influence des facteurs environnementaux sur l’expression des gènes
L’épigénétique apporte un niveau d’explication supplémentaire, mais elle ne doit pas être considérée de manière isolée. Des facteurs environnementaux, allant de la nutrition maternelle à l’exposition à des substances chimiques, peuvent entraîner des modifications chimiques de l’ADN. Ces modifications agissent comme des régulateurs, capables d’augmenter ou de diminuer l’activité de certains gènes. Dans certains cas, elles peuvent influencer les processus neurodéveloppementaux associés au TSA.
Importance du moment : périodes clés du développement cérébral
Les périodes les plus critiques pour ces modifications épigénétiques se situent au cours du premier et du deuxième trimestre de la grossesse. Durant cette phase, le cerveau fœtal connaît une migration et une organisation neuronales rapides. Des perturbations importantes de la régulation génétique pendant ces périodes sensibles peuvent avoir un impact sur le neurodéveloppement.
Obtenez une consultation en ligne gratuite
Chaque cas d’autisme étant unique, une approche individualisée est essentielle. Pour évaluer si la thérapie par cellules souches peut être adaptée à votre enfant, il est possible de planifier une consultation en ligne gratuite avec un spécialiste de Swiss Medica.

Medical Advisor, Swiss Medica doctor
Autisme : facteurs de risque prénatals et de début de vie possibles
Un facteur de risque augmente la probabilité statistique d’un diagnostic, sans constituer une cause directe.
Activation immunitaire maternelle et inflammation
L’une des pistes les plus étudiées parmi l’autisme et ses causes implique la réponse immunitaire de la mère pendant la grossesse. Les infections graves ou les poussées auto-immunes peuvent déclencher une « activation immunitaire maternelle » (AIM). Ce processus libère des protéines inflammatoires appelées cytokines, qui peuvent traverser le placenta et interagir avec le cerveau fœtal, contribuant potentiellement aux profils neuroinflammatoires souvent observés dans le TSA.
Autisme : facteurs de risque liés à un âge parental avancé
Les études montrent de manière constante une association entre un âge parental avancé au moment de la conception et un risque accru de TSA. Cela peut s’expliquer par une fréquence plus élevée de mutations génétiques spontanées dans les cellules germinales avec l’âge, ainsi que par des modifications de la régulation de l’ADN.
Diabète gestationnel et santé métabolique
La santé métabolique maternelle, y compris des conditions telles que le diabète gestationnel et l’obésité, peut créer un environnement intra-utérin altéré. Ces facteurs peuvent influencer le développement fœtal via des mécanismes impliquant la résistance à l’insuline et l’inflammation systémique, constituant ainsi une autre cause potentielle de l’autisme et un facteur de risque lié à la santé prénatale.
Autisme : cause et facteurs environnementaux étudiés
Lorsqu’on se demande quelles sont les causes de l’autisme, « l’environnement » fait référence à tout facteur externe à l’ADN, allant de l’air respiré par la mère aux médicaments pris pendant la grossesse. Les recherches se concentrent sur la manière dont ces facteurs externes peuvent influencer un organisme déjà porteur d’une prédisposition génétique.
Pollution de l’air et exposition aux pesticides pendant la grossesse
Des études épidémiologiques ont suggéré un lien entre l’exposition à des niveaux élevés de particules fines et à certains pesticides pendant la grossesse, et un risque accru de TSA. Ces substances peuvent induire un stress oxydatif ou perturber les signaux hormonaux nécessaires au bon développement du cerveau.
Ce que dit la recherche sur les médicaments pendant la gestation
Certains médicaments, tels que le valproate, ont été associés à des modifications du développement lorsqu’ils sont pris pendant la grossesse. Toutefois, pour la plupart des autres substances, les données restent limitées. Les femmes enceintes doivent toujours consulter un professionnel de santé avant de modifier un traitement prescrit.
Mécanismes biologiques : les processus à l’origine de l’autisme
Les mécanismes biologiques correspondent au « comment », plutôt qu’au « pourquoi ». Dans le cadre de l’autisme et de ses causes, certains facteurs peuvent agir comme déclencheur initial, comme une variation génétique, tandis que les mécanismes biologiques qui suivent participent au développement des caractéristiques et symptômes associés à l’autisme.
Élagage synaptique et différences de connectivité neuronale
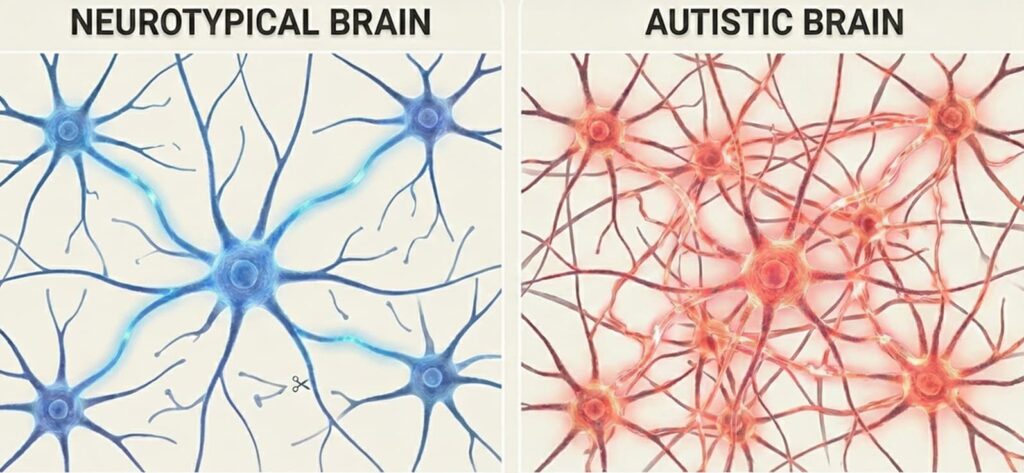
Un cerveau sain passe par un processus appelé « élagage synaptique », au cours duquel les connexions neuronales excédentaires sont éliminées afin d’améliorer l’efficacité.
Dans de nombreux cas, cela constitue une explication biologique de l’autisme chez l’enfant : le processus d’élagage est insuffisant, ce qui conduit à un cerveau « surconnecté ». Cette hyperconnectivité peut expliquer certaines surcharges sensorielles ou des difficultés à traiter des informations sociales complexes.
La neuroinflammation : un domaine de recherche actif
Une inflammation chronique de faible intensité au niveau des cellules immunitaires du cerveau (microglie) est une observation fréquente dans la recherche sur le TSA. Cette neuroinflammation peut perturber l’équilibre chimique nécessaire à la communication neuronale. Même si le déclencheur initial reste inconnu, la gestion de cette inflammation constitue aujourd’hui un axe important des approches biologiques.
Autisme et ses causes : l’axe intestin-cerveau
L’interaction entre l’intestin, le microbiote et le cerveau est activement étudiée dans la recherche sur les causes du TSA, en particulier parce que certains enfants atteints de TSA présentent des troubles gastro-intestinaux. Cependant, les données actuelles ne permettent pas de conclure que les perturbations de l’axe intestin-cerveau sont, à elles seules, responsables de l’autisme.
Différences du microbiote observées chez certaines personnes autistes
Les recherches ont montré que la composition du microbiote intestinal chez les personnes atteintes de TSA diffère souvent de celle des personnes neurotypiques. De nombreux enfants autistes présentent des habitudes alimentaires très sélectives, ce qui peut également influencer la composition du microbiote. Les données actuelles suggèrent donc une corrélation, sans établir de lien causal direct.
Corrélation contre causalité
Bien que les troubles digestifs puissent aggraver la sévérité des symptômes de l’autisme, les chercheurs débattent encore pour déterminer si l’intestin constitue une cause primaire ou une conséquence du trouble. Néanmoins, l’expérience clinique montre qu’une amélioration de la santé digestive est souvent associée à une meilleure concentration et à une diminution de l’irritabilité chez les patients.
Autisme et ses causes : différences métaboliques et mitochondriales étudiées
Le cerveau est l’organe le plus énergivore du corps. Si les cellules ne produisent pas suffisamment d’énergie, les fonctions les plus complexes, comme la communication sociale, peuvent en être affectées.
Métabolisme énergétique et développement cérébral précoce
Les mitochondries sont les « centrales énergétiques » des cellules. Lorsque leur fonctionnement est altéré, on parle de dysfonctionnement mitochondrial. Ce type de dysfonctionnement constitue un facteur important dans certains cas d’autisme, notamment lorsque l’enfant présente des symptômes dits « régressifs », le cerveau pouvant avoir du mal à répondre aux besoins énergétiques élevés du développement précoce.
Autisme et ses causes : stress oxydatif
Le stress oxydatif est un état cellulaire dans lequel les radicaux libres provoquent des dommages, faute d’antioxydants suffisants pour les neutraliser.
- Vulnérabilité du cerveau en développement : le cerveau en développement est sensible au déséquilibre oxydatif car il consomme des niveaux élevés d’oxygène mais possède des défenses antioxydantes relativement plus faibles.
- Un facteur non suffisant : le stress oxydatif n’est pas considéré comme une cause unique ou suffisante du TSA. Au lieu de cela, il est considéré comme un mécanisme secondaire qui peut exacerber les vulnérabilités génétiques existantes, entravant la capacité du cerveau à maintenir un environnement cellulaire sain.
Pourquoi les diagnostics d’autisme augmentent-ils ?
L’augmentation de la prévalence du TSA s’explique principalement par des évolutions dans les pratiques cliniques et une meilleure sensibilisation, plutôt que par une modification soudaine de la biologie humaine.
Meilleure sensibilisation et critères diagnostiques élargis
La principale raison de la hausse des diagnostics réside dans l’adoption de la notion de « spectre », qui permet d’inclure des profils plus variés, notamment des formes plus légères qui n’auraient pas été diagnostiquées auparavant.
Ce qu’une prévalence croissante signifie et ne signifie pas
Une prévalence plus élevée signifie que davantage de personnes accèdent au soutien dont elles ont besoin. Cela ne signifie pas qu’il existe une « épidémie » biologique liée aux modes de vie modernes, mais reflète plutôt une meilleure capacité à identifier la neurodivergence.
Autisme et ses causes chez l’enfant : démystifier les idées reçues
La désinformation peut engendrer une culpabilité inutile chez les familles. La science a clairement écarté les facteurs suivants comme cause du TSA :
Vaccins
Depuis des décennies, le lien supposé entre les vaccins et l’autisme figure parmi les mythes les plus persistants en médecine. Cependant, des données cliniques approfondies, portant sur des millions d’enfants dans le monde, ont démontré de manière concluante l’absence de relation de causalité entre les vaccinations (comme le vaccin ROR) et le développement du TSA. La recherche actuelle se concentre sur des facteurs génétiques et prénatals, plutôt que sur des déclencheurs externes tels que la vaccination.
Styles parentaux
Historiquement, la théorie de la « mère réfrigérateur » suggérait qu’un manque de chaleur maternelle pouvait être à l’origine de l’autisme. Cette hypothèse a été totalement réfutée par la psychologie moderne. L’autisme est aujourd’hui reconnu comme un trouble neurodéveloppemental d’origine biologique, et aucune preuve ne permet d’établir un lien avec les styles parentaux ou la dynamique familiale.
Facteurs alimentaires
Bien que de nombreux parents aient recours à des régimes sans gluten ou sans caséine pour atténuer certains troubles gastro-intestinaux associés, la science est claire : l’alimentation seule n’est pas une cause de l’autisme. Les interventions nutritionnelles peuvent contribuer au bien-être général de l’enfant. Toutefois, le TSA repose sur des mécanismes liés à la connectivité cérébrale et au développement neurologique, qui ne peuvent ni être déclenchés ni « guéris » uniquement par des modifications alimentaires.
Des causes de l’autisme à l’accompagnement : ce que la compréhension biologique permet d’orienter
Lorsqu’une famille comprend les causes biologiques de l’autisme, elle peut s’orienter vers un plan de soins multidisciplinaire plus efficace. Les causes de l’autisme (Asperger et autres formes) sont reconnues comme complexes, nécessitant un accompagnement global. Cela comprend :
- Un accompagnement précoce : tirer parti de la plasticité cérébrale dès les premières années.
- Des soins individualisés : cibler des marqueurs métaboliques ou inflammatoires spécifiques.
- La prise en compte des troubles associés : recourir à l’orthophonie pour l’autisme et la thérapie comportementale pour l’autisme afin de s’appuyer sur une base biologique plus stable.
Thérapies régénératives et biologiques en cours d’étude
Les chercheurs explorent des approches visant à moduler la neuroinflammation et les dérégulations du système immunitaire, fréquemment observées dans le TSA.
Pourquoi les voies immunitaires et inflammatoires sont étudiées
Étant donné que de nombreux enfants atteints de TSA présentent des signes d’inflammation systémique, la recherche médicale s’intéresse à des thérapies susceptibles de « calmer » le système immunitaire et de favoriser un environnement neuronal plus stable.
La recherche sur les cellules souches comme piste exploratoire
Nous considérons la recherche sur les cellules souches comme l’un des nombreux moyens de mieux comprendre et de soutenir les besoins biologiques des personnes sur le spectre. Actuellement, les scientifiques explorent comment la thérapie par cellules souches pour l’autisme pourrait aider à équilibrer les réponses inflammatoires naturelles du corps, créant potentiellement un environnement interne plus calme.
Comment les cellules souches mésenchymateuses sont étudiées pour la modulation immunitaire et inflammatoire
Les cellules souches mésenchymateuses (CSM) sont étudiées pour leur capacité à libérer des cytokines anti-inflammatoires. Dans le contexte du TSA, elles pourraient contribuer à moduler une réponse immunitaire excessive, avec des effets potentiels sur l’engagement social et la communication.
Mécanisme d’action : la neuroinflammation pourrait être réduite via l’inhibition de l’activation microgliale et la diminution de la production de cytokines pro-inflammatoires. La régulation immunitaire passerait notamment par la modulation des interactions HLA, de la reconnaissance des cellules T et par un basculement vers des profils immunitaires anti-inflammatoires (Th et macrophages).
Profil de sécurité : les perfusions intraveineuses de CSM issues du cordon ombilical ont été globalement bien tolérées chez des enfants et des adultes atteints de TSA, sans événements indésirables graves, réactions à la perfusion ou complications inattendues rapportées dans plusieurs études.
L’approche de Swiss Medica pour une prise en charge individualisée, fondée sur la biologie
Chez Swiss Medica, nous privilégions une évaluation globale, dite « du corps entier ». L’objectif est d’identifier et de prendre en compte les déséquilibres biologiques sous-jacents susceptibles de freiner les progrès du patient.
Évaluation médicale et développementale complète
Chaque patient fait l’objet d’un bilan incluant le dépistage de troubles métaboliques, d’inflammation chronique et de carences nutritionnelles, afin de mieux comprendre son profil biologique spécifique.
Plan de traitement individualisé
Sur la base des résultats diagnostiques, un protocole personnalisé est élaboré. Il ne s’agit pas d’une approche standardisée.
La thérapie par cellules souches comme option de soutien
Dans notre clinique, nous proposons des thérapies basées sur les cellules souches mésenchymateuses (CSM), envisagées comme un outil de soutien visant notamment à agir sur la neuroinflammation et à accompagner les processus naturels de régénération de l’organisme. Cette approche s’inscrit dans un programme intégré et multidisciplinaire :
- Administration cellulaire multimodale : le protocole inclut l’administration intraveineuse et intramusculaire de cellules souches issues du cordon ombilical et du placenta, sélectionnées pour leurs propriétés anti-inflammatoires et régénératrices.
- Thérapies synergiques en clinique : pour améliorer l’efficacité des cellules souches et traitements proposés, le programme peut inclure des thérapies par exosomes et macrophages. Ces agents biologiques agissent comme des « messagers », en stimulant les mécanismes naturels de réparation et en contribuant à réguler les voies inflammatoires.
Thérapies de soutien intégrées
Pour favoriser les progrès du patient, le programme Swiss Medica associe des interventions médicales avancées à un ensemble de thérapies de soutien. Celles-ci sont intégrées directement au séjour en clinique afin de tirer parti de la fenêtre d’opportunité ouverte par la thérapie cellulaire. Elles comprennent notamment :
- Orthophonie
- Ergothérapie
- Supplémentation ciblée
Suivi, surveillance et soins continus
À leur sortie, les familles reçoivent des préparations d’exosomes et de sécrétome M2 destinées à une utilisation à domicile. Cette approche vise à soutenir, dans la durée, les mécanismes anti-inflammatoires et à prolonger les effets observés pendant la phase en clinique. La prise en charge s’inscrit dans le temps et ne se limite pas à une intervention ponctuelle. L’équipe reste en contact régulier avec les familles afin de suivre l’évolution, d’observer les progrès développementaux et d’apporter des recommandations en matière de nutrition et de thérapies de soutien au fil du parcours de l’enfant.
Faites le premier pas vers une stratégie de prise en charge régénérative
Le profil biologique de chaque enfant est unique. Lors d’une consultation avec nos spécialistes, nous évaluons comment adapter les options régénératives intensives au stade fonctionnel actuel de votre enfant.
Lors de cette évaluation, nous discuterons :
- L’historique de régression de votre enfant et ses marqueurs biologiques spécifiques.
- La pertinence du programme dans son cas.
- Le rôle des thérapies de soutien, telles que l’oxygénothérapie hyperbare (OHB) et la supplémentation ciblée.

Medical Advisor, Swiss Medica doctor
Ce que les familles et les équipes de soins observent le plus souvent après une thérapie par cellules souches
Selon un essai clinique mené par Swiss Medica auprès de 30 enfants atteints de TSA sur une période de 9 mois, une majorité de familles ont rapporté des évolutions positives dans le quotidien de leur enfant. L’étude indique que 93,4 % des patients ont présenté une amélioration mesurable d’au moins un symptôme principal, tandis que 83,3 % ont progressé sur la moitié ou plus de leurs symptômes.
Les équipes de soins et les parents ont le plus fréquemment signalé des améliorations dans les domaines suivants :
- Communication sociale : un meilleur contact visuel et un plus grand désir d’interagir avec les autres.
- Régulation comportementale : une réduction notable de l’hyperactivité et des accès d’agressivité.
- Compétences cognitives : une amélioration de la capacité d’attention et de meilleures performances dans l’apprentissage de nouvelles tâches.
- Fonctionnement quotidien : des progrès dans les routines de soins personnels et des habitudes de sommeil plus stables.
L’histoire de notre patient
La mère d’Uval s’est rendue chez Swiss Medica après avoir constaté une régression sévère chez son fils. À l’âge de trois ans, Uval atteignait les étapes de développement attendues, mais à quatre ans, il a présenté ce que sa famille a décrit comme un « autisme régressif ». Il a cessé de parler et s’est comme effacé.
« Nous l’avons perdu soudainement à l’âge de quatre ans. Nous avons essayé l’orthophonie, l’ABA et des médicaments, sans aucun effet. Après être venus chez Swiss Medica, nous avons constaté une réelle amélioration. Environ trois semaines après le traitement, il a recommencé à nous appeler “maman” et “papa”. Aujourd’hui, il peut former des phrases complètes. Il est plus présent. Notre quotidien a changé, car nous pouvons enfin communiquer avec notre enfant. »
Vous pouvez en apprendre davantage sur les témoignages de patients et leurs expériences avec la thérapie par cellules souches. La chaîne YouTube officielle de Swiss Medica propose une liste de lecture dédiée à la prise en charge de l’autisme.
Prochaines étapes pratiques pour les familles après avoir compris les causes de l’autisme
Comprendre les composantes biologiques de l’autisme fournit une véritable feuille de route pour passer à l’action.
- Discuter des préoccupations avec les cliniciens : recherchez des spécialistes qui adoptent une approche globale de l’enfant, en se concentrant sur des facteurs systémiques tels que la neuroinflammation, la santé gastro-intestinale et l’équilibre métabolique, plutôt qu’uniquement sur les symptômes comportementaux.
- Éviter le blâme ou la culpabilité : rappelez-vous que l’autisme est une réalité biologique complexe, souvent liée à la neuroinflammation et à des facteurs génétiques, et non le résultat de choix parentaux ou de la dynamique familiale.
- Demander une consultation spécialisée : consultez un expert en médecine régénérative chez Swiss Medica afin d’explorer comment nos protocoles de soutien biologique peuvent compléter la prise en charge actuelle de votre enfant et améliorer sa qualité de vie.
- Privilégier les cliniques axées sur la sécurité : si vous envisagez une approche régénérative, choisissez une clinique qui applique des normes de sécurité strictes. Il est essentiel de s’assurer que l’établissement, comme Swiss Medica, respecte des protocoles rigoureux pour le dépistage, la culture et l’administration des cellules, afin de garantir le plus haut niveau de sécurité des soins.
Contactez-nous
Si vous souhaitez mieux comprendre le profil biologique unique de votre enfant, notre équipe est à votre disposition.

Medical Advisor, Swiss Medica doctor
Foire aux questions
1. L’identification des causes du TSA peut-elle modifier la prise en charge ?
Oui. L’identification de facteurs biologiques, comme une dysbiose intestinale, permet de mettre en place des interventions ciblées pouvant améliorer la concentration, le confort et la capacité de l’enfant à s’engager dans des thérapies traditionnelles.
2. Comprendre la biologie signifie-t-il que l’autisme peut être guéri ?
Non. L’objectif du soutien biologique est d’atténuer les symptômes les plus contraignants et d’aider la personne à atteindre son plein potentiel.
3. La thérapie par cellules souches modifie-t-elle la structure du cerveau ?
La thérapie par cellules souches est étudiée pour sa capacité à moduler l’environnement biologique (notamment l’inflammation), et non à « réécrire » le code génétique du cerveau.
4. Combien de temps faut-il pour observer des changements après une thérapie par cellules souches ?
Chaque enfant est différent, mais des améliorations fonctionnelles, notamment au niveau du langage ou des interactions sociales, apparaissent généralement dans un délai de 3 à 6 mois.
5. Les améliorations après une thérapie par cellules souches sont-elles permanentes ?
La thérapie ouvre une période durant laquelle le cerveau est particulièrement réceptif à l’apprentissage. Les compétences acquises et les progrès réalisés pendant cette phase (comme de nouvelles capacités de communication ou des comportements sociaux) peuvent constituer une base durable. Cependant, chaque intervention correspond à une étape spécifique : pour poursuivre les progrès et atteindre un niveau de développement supérieur, des administrations supplémentaires de cellules peuvent être nécessaires.
Liste des Références:
Lim HK, Yoon JH, Song M. Gènes du trouble du spectre de l’autisme : réseaux liés à la maladie et stratégies compensatoires. Front Mol Neurosci. 2022;15:922840. doi:10.3389/fnmol.2022.922840.
Bai D, Yip BHK, Windham GC, et al. Association des facteurs génétiques et environnementaux avec l’autisme dans une cohorte de 5 pays. JAMA Psychiatry. 2019;76(10):1035-1043. doi:10.1001/jamapsychiatry.2019.1411.
Yoon S, Munoz A, Yamrom B, et al. Taux de mutations de novo contributives dans les familles à haut et faible risque d’autisme. Commun Biol. 2021;4:1026. doi:10.1038/s42003-021-02533-z.
Tick B, Bolton P, Happé F, Rutter M, Rijsdijk F. Héritabilité des troubles du spectre de l’autisme : une méta-analyse d’études sur des jumeaux. J Child Psychol Psychiatry. 2016 May;57(5):585-595. doi:10.1111/jcpp.12499.
Keil KP, Lein PJ. Méthylation de l’ADN : un mécanisme reliant les expositions aux produits chimiques environnementaux au risque de troubles du spectre de l’autisme ? Environ Epigenet. 2016 Mar;2(1):dvv012. doi:10.1093/eep/dvv012.
Ellul P, Maruani A, Vantalon V, et al. L’activation immunitaire maternelle pendant la grossesse est associée à davantage de difficultés dans les comportements socio-adaptatifs au sein du trouble du spectre de l’autisme. Sci Rep. 2023;13:17687. doi:10.1038/s41598-023-45060-z.
Wu S, Wu F, Ding Y, Hou J, Bi J, Zhang Z. Âge parental avancé et risque d’autisme chez les enfants : une revue systématique et méta-analyse. Acta Psychiatr Scand. 2017 Jan;135(1):29-41. doi:10.1111/acps.12666.
Pagalan L, Bickford C, Weikum W, et al. Association de l’exposition prénatale à la pollution de l’air avec le trouble du spectre de l’autisme. JAMA Pediatr. 2019;173(1):86-92. doi:10.1001/jamapediatrics.2018.3101.
Harden CL. Exposition au valproate in utero et autisme : longtemps suspectée, enfin prouvée. Epilepsy Curr. 2013 Nov;13(6):282-284. doi:10.5698/1535-7597-13.6.282.
Andreo-Martínez P, Rubio-Aparicio M, Sánchez-Meca J, Veas A, Martínez-González AE. Une méta-analyse du microbiote intestinal chez les enfants atteints d’autisme. J Autism Dev Disord. 2022 Mar;52(3):1374-1387. doi:10.1007/s10803-021-05002-y.
DeStefano F, Shimabukuro TT. Le vaccin ROR et l’autisme. Annu Rev Virol. 2019 Sep 29;6(1):585-600. doi:10.1146/annurev-virology-092818-015515.
Paprocka J, Kaminiów K, Kozak S, Sztuba K, Emich-Widera E. Thérapies par cellules souches pour la paralysie cérébrale et le trouble du spectre de l’autisme – Une revue systématique. Brain Sci. 2021 Dec 3;11(12):1606. doi:10.3390/brainsci11121606.
Tamouza R, Volt F, Richard JR, Wu CL, Bouassida J, Boukouaci W, Lansiaux P, Cappelli B, Scigliuolo GM, Rafii H, Kenzey C, Mezouad E, Naamoune S, Chami L, Lejuste F, Farge D, Gluckman E. Effet possible de l’utilisation de cellules stromales mésenchymateuses dans le traitement des troubles du spectre de l’autisme : une revue. Front Cell Dev Biol. 2022 Jul 5;10:809686. doi:10.3389/fcell.2022.809686.
MD, Pediatrician, Regenerative Medicine Specialist